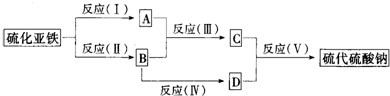
A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系知图所示.

请回答下列问题:
(1)若D为用量最大、用途最广的金属单质,加热蒸干B的溶液没有得到B的盐,则B的化学式可能为
FeCl3或Fe(NO3)3
FeCl3或Fe(NO3)3
.(写出一种即可)
(2)若通常情况下A、B、C、D都是气体,且B和D为空气的主要成分,则A的电子式为
,B的结构式为
N≡N
N≡N
.
(3)若D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式为
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.
(4)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一,也可作为医疗上治疗胃酸过多症的药剂.
①25℃时,pH均为10的A、B两溶液中,由水电离出的氢氧根离子浓度之比为
10-6:1或1:106
10-6:1或1:106
②25℃时,0.1mol?L
-1的A、B、C三种溶液,分别用水稀释不同的倍数后,溶液的pH相同,则稀释后溶液的物质的量浓度最大的是
NaHCO3
NaHCO3
溶液(填溶质的化学式).
③将等物质的量的B和C溶于水形成混合溶液,溶液中各种离子浓度由大到小顺序为
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
.




 ,B为N2,结构式为N≡N,故答案为:
,B为N2,结构式为N≡N,故答案为: ;N≡N;
;N≡N;

 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图所示(部分反应中的水已略去).
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图所示(部分反应中的水已略去). Fe(OH)3+3H+
Fe(OH)3+3H+ Fe(OH)3+3H+
Fe(OH)3+3H+