
| A. | “类钫”属过渡元素,具有放射性 | B. | “类钫”可与水剧烈反应 | ||
| C. | “类钫”单质的密度小于1g/cm3 | D. | “类钫”单质有较高熔点 |
分析 119号“类钫”是第8周期ⅠA族的元素,其金属性在第IA族最强,根据同一主族元素的性质具有相似性和递变性来解答.
解答 解:A.119号“类钫”是第8周期ⅠA族的元素,所以不是过渡元素,但具有放射性,故A错误;
B.Cs和水剧烈反应,类钫其金属性更强,所以与水剧烈反应,故B正确;
C.碱金属从上到下,单质的密度呈增大趋势,“类钫”的密度应大于1 g/cm3,故D错误;
B.碱金属族元素单质的熔沸点随着原子序数增大而减小,所以“类钫”单质熔沸点较低,故D错误;
故选B.
点评 本题考查元素性质,侧重考查知识迁移能力,根据同一主族元素性质递变规律采用知识迁移的方法进行解答,题目难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:填空题
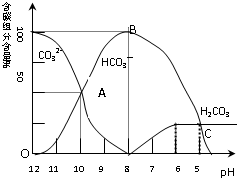 常温下在20mL0.1mol/L碳酸钠溶液中逐滴加入0.1mol/L盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒的百分含量也发生变化(二氧化碳因为逸出未画出).据此回答下列问题:
常温下在20mL0.1mol/L碳酸钠溶液中逐滴加入0.1mol/L盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒的百分含量也发生变化(二氧化碳因为逸出未画出).据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F六种物质的相互转化关系如附图所示(反应条件未标出).
A、B、C、D、E、F六种物质的相互转化关系如附图所示(反应条件未标出).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子组成中相差一个或几个CH2 原子团的有机物是同系物 | |
| B. | 各组成元素质量分数相同的烃是同一种烃 | |
| C. | 分子式相同而结构不同的有机物不一定是同分异构体 | |
| D. | 互为同系物的有机物其分子结构必然相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z>W | B. | 金属性:X<Y,还原性:W 2->Z- | ||
| C. | 原子最外层电子数:Y>X>Z>W | D. | 原子序数:Y>X>Z>W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锥形瓶里溶液在滴定过程中溅出 | |
| B. | 滴定管装液后尖嘴部位有气泡,滴定后气泡消失 | |
| C. | 指示剂变色15s后又恢复为原来的颜色便停止滴定 | |
| D. | 锥形瓶用蒸馏水冲洗后未用待测液润洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 40% | C. | 50% | D. | 60% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com