
分析 乙烯为原料可合成乙二酸二乙酯,要先制得乙醇和乙二酸,乙二酸可由乙烯通过加成、水解、氧化制得,乙醇可由乙烯与水加成制得,据此写出化学方程式.
解答 解:以乙醇为原料合成乙二酸乙二酯,
经过以下几步第一步:乙烯与溴发生加成反应生成1,2-二溴乙烷,方程式:CH2=CH2+Br2→CH2BrCH2Br;
第二步:1,2-二溴乙烷水解生成乙二醇,方程式:CH2BrCH2Br+2NaOH$→_{△}^{水}$CH2OHCH2OH+2NaBr;
第四步:乙二醇氧化生成乙二酸,方程式:CH2OHCH2OH+2O2$\stackrel{一定条件下}{→}$HOOC-COOH+2H2O;
第五步:HOCH2CH2OH与乙二酸发生酯化反应生成环状化合物的化学方程式为: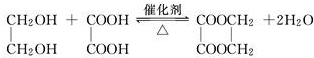 ,
,
故答案为:CH2=CH2+Br2→CH2BrCH2Br;CH2BrCH2Br+2NaOH$→_{△}^{水}$CH2OHCH2OH+2NaBr;CH2OHCH2OH+2O2$\stackrel{一定条件下}{→}$HOOC-COOH+2H2O; .
.
点评 本题为有机合成题,明确物质的结构及性质是解题关键,注意方程式书写的注意问题,题目难度不大.


科目:高中化学 来源: 题型:填空题
 由于受3d电子的影响,元素周期表中第四周期过渡元素的明显特征是形成多种多样的配合物.
由于受3d电子的影响,元素周期表中第四周期过渡元素的明显特征是形成多种多样的配合物. 分子内的作用力没有B (填编号).
分子内的作用力没有B (填编号).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
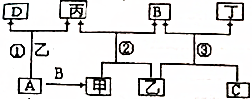 2:1.
2:1.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol H2与0.5mol H2和O2的混合物所含的原子数目相同 | |
| B. | 32g O2含有6.02×1023个氧分子 | |
| C. | 1mol H2O中含有2mol H2,1mol O,总共所含电子的物质的量为10mol | |
| D. | 物质的量为1mol 的任何微粒的质量与NA个该种微粒的质量在任何情况下都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | CO | CO2 | C2H6 | NOx | 焦油 | 尼古丁 | 甲醛 | 苯 |
| 含量 (mg/支) | 17 | 60 | 0.6 | 0.6 | 35 | 2.5 | 0.05 | 0.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com