
әмИИөДМъДЬУлЛ®ХфЖш·ҙУҰЈ¬УРЗвЖшЙъіЙЈ¬ПЦУГИзНјЛщКҫЧ°ЦГҪшРРМъФЪёЯОВПВУлЛ®ХфЖш·ҙУҰөДКөСйЈ¬ІўУГјтөҘөД·Ҫ·ЁКХјҜЎўјмСйЙъіЙөДЗвЖшЎЈЗл»ШҙрПВБРОКМвЈә
(1)РҙіцМъФЪёЯОВПВУлЛ®ХфЖш·ҙУҰөД»ҜС§·ҪіМКҪЈә ЎЈ
(2)ёЙФп№ЬCДЪКў·ЕөДТ©Ж·КЗ әН (Мо»ҜС§КҪ)ЎЈёЙФп№ЬөД (МоЎ°mЎұ»тЎ°nЎұ)¶ЛУлgөј№ЬПаБ¬ҪУЎЈ

(3)ФЪDҙҰ»ӯіцУГКФ№ЬКХјҜЗвЖшөДЧ°ЦГНј(ЛщРиЖдЛыТЗЖчЧФРРСЎФс)ЎЈ
(4)ФхСщУГјтөҘөД·Ҫ·ЁјмСйКХјҜөҪөДЖшМеКЗЗвЖшЈ¬јтКцКөСйІЩЧчІҪЦиәНПЦПу ЎЈ
(1)3FeЈ«4H2O(g)  Fe3O4Ј«4H2 (2)CaCl2 CaO n
Fe3O4Ј«4H2 (2)CaCl2 CaO n
(3)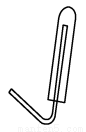
(4)УГДҙЦё¶ВЧЎКФ№ЬҝЪЈ¬КФ№ЬҝЪПтЙПЈ¬ҝҝҪьҫЖҫ«өЖ»рСжЈ¬ЛЙҝӘДҙЦёЈ¬ДЬИјЙХ»т·ўіцұ¬ГщЙщЈ¬ЛөГчКХјҜөДКЗH2ЎЈ
ЎҫҪвОцЎҝ
КФМв·ЦОцЈәўЕМъФЪёЯОВПВУлЛ®ХфЖш·ҙУҰөД»ҜС§·ҪіМКҪЈә3FeЈ«4H2O(g)  Fe3O4Ј«4H2 Ј»ўЖЧ°ЦГК№УГёЙФп№ЬКЗёЙФпЗвЖшЦРөДЛ®ХфЖшЈ¬ёЙФп№ЬЦРҝЙЧ°І»УлH2·ҙУҰөДёЙФпјБЈ¬ИзCaCl2ЎўCaOөИЈ¬ёЙФп№ЬЦРЖшМеУҰҙУҙу№ЬҪшЈ¬РЎ№ЬіцЈ¬ЛщТФn¶ЛУлgөј№ЬПаБ¬ҪУ
Fe3O4Ј«4H2 Ј»ўЖЧ°ЦГК№УГёЙФп№ЬКЗёЙФпЗвЖшЦРөДЛ®ХфЖшЈ¬ёЙФп№ЬЦРҝЙЧ°І»УлH2·ҙУҰөДёЙФпјБЈ¬ИзCaCl2ЎўCaOөИЈ¬ёЙФп№ЬЦРЖшМеУҰҙУҙу№ЬҪшЈ¬РЎ№ЬіцЈ¬ЛщТФn¶ЛУлgөј№ЬПаБ¬ҪУ
ўЗH2ГЬ¶ИРЎУЪҝХЖшЈ¬УҰУГПтПВЕЕҝХ·ЁКХјҜЈ¬УГКФ№ЬКХјҜЗвЖшөДЧ°ЦГНјОӘ ўИјмСйКХјҜөҪөДЖшМеКЗЗвЖшЈ¬ІЩЧчОӘЈәУГДҙЦё¶ВЧЎКФ№ЬҝЪЈ¬КФ№ЬҝЪПтЙПЈ¬ҝҝҪьҫЖҫ«өЖ»рСжЈ¬ЛЙҝӘДҙЦёЈ¬ДЬИјЙХ»т·ўіцұ¬ГщЙщЈ¬ЛөГчКХјҜөДКЗH2Ј¬ҙр°ёЈәУГДҙЦё¶ВЧЎКФ№ЬҝЪЈ¬КФ№ЬҝЪПтЙПЈ¬ҝҝҪьҫЖҫ«өЖ»рСжЈ¬ЛЙҝӘДҙЦёЈ¬ДЬИјЙХ»т·ўіцұ¬ГщЙщЈ¬ЛөГчКХјҜөДКЗH2ЎЈ
ўИјмСйКХјҜөҪөДЖшМеКЗЗвЖшЈ¬ІЩЧчОӘЈәУГДҙЦё¶ВЧЎКФ№ЬҝЪЈ¬КФ№ЬҝЪПтЙПЈ¬ҝҝҪьҫЖҫ«өЖ»рСжЈ¬ЛЙҝӘДҙЦёЈ¬ДЬИјЙХ»т·ўіцұ¬ГщЙщЈ¬ЛөГчКХјҜөДКЗH2Ј¬ҙр°ёЈәУГДҙЦё¶ВЧЎКФ№ЬҝЪЈ¬КФ№ЬҝЪПтЙПЈ¬ҝҝҪьҫЖҫ«өЖ»рСжЈ¬ЛЙҝӘДҙЦёЈ¬ДЬИјЙХ»т·ўіцұ¬ГщЙщЈ¬ЛөГчКХјҜөДКЗH2ЎЈ
ҝјөгЈәМъј°Жд»ҜәПОпөДРФЦККөСй


 »оБҰҝОКұН¬ІҪБ·П°ІбПөБРҙр°ё
»оБҰҝОКұН¬ІҪБ·П°ІбПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмҪӯОчКЎИэКРЛДРЈёЯТ»ЙПС§ЖЪЖЪД©БӘҝј»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәМоҝХМв
ЈЁ1Ј©КөСйКТУГВИ»Ҝ粒ММеЦЖИЎ°ұЖшөД»ҜС§·ҪіМКҪКЗ ЎЈ
ЈЁ2Ј©Ҫ«4.48LЈЁұкЧјЧҙҝцЈ©°ұЖшНЁИлЛ®ЦРөГөҪ0.05LИЬТәЈ¬ЛщөГИЬТәөДОпЦКөДБҝЕЁ¶ИКЗ ЎЈ
ЈЁ3Ј©ПЦУР100mL AlCl3УлMgSO4өД»мәПИЬТәЈ¬·ЦіЙБҪөИ·ЭЎЈ
ўЩПтЖдЦРТ»·ЭЦРјУИл10mL 4mol/LөД°ұЛ®Ј¬ЗЎәГНкИ«·ҙУҰЈ¬ЖдЦРAlCl3Ул°ұЛ®·ҙУҰөДАлЧУ·ҪіМКҪКЗ ЎЈјМРшјУИлl mol/L NaOHИЬТәЦБ10mLКұЈ¬іБөнІ»ФЩјхЙЩЈ¬іБөнјхЙЩөДАлЧУ·ҪіМКҪКЗ Ј¬јхЙЩөДіБөнөДОпЦКөДБҝКЗ ЎЈ
ўЪПтБнТ»·ЭЦРјУИлa mL 1mol/LBaCl2ИЬТәДЬК№SO42ЈӯіБөнНкИ«Ј¬a= ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмҪӯЛХКЎЙПС§ЖЪЖЪЦРҝјКФёЯТ»»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ДіәПЧчС§П°РЎЧйМЦВЫұжОцТФПВЛө·ЁЈәўЩұщЛ®»мәПОпәНЛбУк¶јКЗ»мәПОпЈ»ўЪЛ®ГәЖшәНКҜУН¶јКЗҝЙФЩЙъДЬФҙЈ»ўЫІ»РвёЦәНДҝЗ°БчНЁөДУІұТ¶јКЗәПҪрЈ»ўЬПЎБтЛбәНКіҙЧјИКЗ»ҜәПОпУЦКЗЛбЈ»ўЭҙҝјоәНКмКҜ»Т¶јКЗјоЈ»ўЮөн·ЫИЬТәәНОн¶јКЗҪәМеЎЈЙПКцЛө·ЁХэИ·өДКЗ
AЈ®ўЫўЬ BЈ®ўЫўЮ CЈ®ўЩўЫўЭ DЈ®ўЩўЫўЮ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмҪӯЛХКЎ»ҙ°ІКРҪМС§РӯЧчМеёЯТ»ЙПС§ЖЪЖЪД©»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
Ў°ВМЙ«»ҜС§ЎұКЗЦёҙУјјКхЎўҫӯјГЙПЙијЖҝЙРРөД»ҜС§·ҙУҰЈ¬ҫЎҝЙДЬјхЙЩ¶Ф»·ҫіөДёұЧчУГЎЈПВГж»ҜС§·ҙУҰІ»·ыәПВМЙ«»ҜС§ёЕДоөДКЗ
AЈ®ПыіэБтЛбі§ОІЖшЕЕ·ЕЈәSO2Ј«2NH3 = (NH4)2SO3
BЈ®ПыіэЦЖПхЛб№ӨТөОІЖшЕЕ·ЕЈәNO2Ј«NOЈ«2NaOH =2NaNO2Ј«H2O
CЈ®ЦЖCuSO4ЈәCuЈ«2H2SO4(ЕЁ) = CuSO4Ј«SO2ЎьЈ«2H2O
DЈ®ЦЖCuSO4Јә2CuЈ«O2= 2CuO CuOЈ«H2SO4(ПЎ) = CuSO4Ј«H2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмҪӯЛХКЎ»ҙ°ІКРҪМС§РӯЧчМеёЯТ»ЙПС§ЖЪЖЪД©»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБРЖшМеЕЕИлҙуЖшЈ¬І»»бФміЙҝХЖшОЫИҫөДКЗЈЁ Ј©
AЈ®N2 BЈ®SO2 CЈ®C12 DЈ®NO
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмҪӯЛХКЎМ©ЦЭКРҪӘСЯЗшёЯТ»ЙПС§ЖЪЖЪЦРҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ОӘБЛіэИҘҙЦСОЦРөДCa2+ЎўMg2+ЎўSO42-ј°ДаЙіЈ¬ҝЙҪ«ҙЦСОИЬУЪЛ®Ј¬И»әуҪшРРПВБРОеПоІЩЧчЈәўЩ№эВЛЈ»ўЪјУ№эБҝNaOHИЬТәЈ»ўЫјУККБҝСОЛбЈ»ўЬјУ№эБҝNa2CO3ИЬТәЈ»ўЭјУ№эБҝBaCl2ИЬТәЎЈІ»ХэИ·өДІЩЧчЛіРтКЗ
AЈ®ўЩўЬўЪўЭўЫ BЈ®ўЭўЬўЪўЩўЫ CЈ®ўЪўЭўЬўЩўЫ DЈ®ўЭўЪўЬўЩўЫ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмҪӯЛХКЎМ©ЦЭКРҪӘСЯЗшёЯТ»ЙПС§ЖЪЖЪЦРҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБР·ҙУҰөДАлЧУ·ҪіМКҪКйРҙХэИ·өДКЗ
AЈ®ВИ»ҜНӯИЬТәУлМъ·Ы·ҙУҰЈәCu2+ + Fe = Fe2+ + Cu
BЈ®ПЎH2SO4УлМъ·Ы·ҙУҰЈә2Fe + 6H+ = 2Fe3+ + 3H2Ўь
CЈ®ЗвСх»ҜұөИЬТәУлПЎH2SO4·ҙУҰЈәBa2+ + SO42Јӯ= BaSO4Ўэ
DЈ®МјЛбёЖУлСОЛб·ҙУҰЈәCO32Јӯ+ 2H+ = H2O + CO2Ўь
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмҪӯЛХКЎгрСфПШёЯТ»ЙПС§ЖЪЖЪЦРҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәМоҝХМв
әйФЦ№эәуЈ¬ТыУГЛ®өДПы¶ҫЙұҫъіЙОӘТЦЦЖҙу№жДЈҙ«ИҫРФјІІЎұ¬·ўөДУРР§·Ҫ·ЁЦ®Т»ЎЈЖҜ°Ч·ЫКЗіЈУГөДПы¶ҫјБЦ®Т»ЎЈ
ЈЁ1Ј©№ӨТөЙПҪ«ВИЖшНЁИлКҜ»ТИй[Ca(OH)2]ЦЖИЎЖҜ°Ч·ЫЈ¬»ҜС§·ҙУҰ·ҪіМКҪОӘ ЈЁ·ҙУҰўЩЈ©ЎЈ
ЈЁ2Ј©ЖҜ°Ч·ЫИЬУЪЛ®әуЈ¬КЬҝХЖшЦРөДCO2ЧчУГЈ¬јҙІъЙъУРЖҜ°ЧЎўЙұҫъЧчУГөДҙОВИЛбЈ¬·ҙУҰ»ҜС§·ҪіМКҪОӘ ЈЁ·ҙУҰўЪЈ©ЎЈ
ЈЁ3Ј©ҙОВИЛбІ»ОИ¶ЁЈ¬ИЭТЧ·ЦҪвЈ¬»ҜС§·ҙУҰ·ҪіМКҪОӘ ЈЁ·ҙУҰўЫЈ©ЎЈ
ЈЁ4Ј©·ҙУҰўЩЎў·ҙУҰўЪЎў·ҙУҰўЫЦРЈ¬КфУЪСх»Ҝ»№Фӯ·ҙУҰөДКЗЈЁМо·ҙУҰұаәЕЈ© ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2016ҪмҪӯЛХКЎёЯТ»ЙПС§ЖЪЖЪЦРҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
КөСйКТРиУГ480mL0.5mol/LөДNaOHИЬТәЈ¬Ј¬ТФПВІЩЧчХэИ·өДКЗ
AЈ®іЖИЎ10.0gNaOHЈ¬јУИл500mLЛ®
BЈ®іЖИЎ10.0gNaOHЈ¬СЎИЎ500mLИЭБҝЖҝҪшРРЕдЦЖ
CЈ®іЖИЎ9.6gNaOHЈ¬СЎИЎ480mLИЭБҝЖҝҪшРРЕдЦЖ
DЈ®іЖИЎ9.6gNaOHЈ¬СЎИЎ500mLИЭБҝЖҝҪшРРЕдЦЖ
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com