
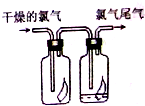
 如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到右瓶的现象是:有色布条褪色,发生此现象的原因是Cl2+H2O?HCl+HClO.(用有关的方程式解释)
如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到右瓶的现象是:有色布条褪色,发生此现象的原因是Cl2+H2O?HCl+HClO.(用有关的方程式解释)  名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:3:2 | B. | 5:5:4 | C. | 2:2:3 | D. | 1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水中滴加石蕊试液显蓝色 | |
| B. | NO2通入水中,气体由红棕色逐渐转变为无色 | |
| C. | 萃取时向碘水中滴加适量的稀盐酸,有透明的凝胶形成 | |
| D. | 向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎将浓碱溶液沾到皮肤上,立即用大量硫酸冲洗,然后再用水冲洗 | |
| B. | 不慎将酸溅到眼中,立即用大量水冲洗,边洗边眨眼睛 | |
| C. | 实验时手指上不小心沾上浓硫酸,立即用NaOH溶液清洗 | |
| D. | 酒精不慎洒在实验桌上烧起来时,立即用水浇灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
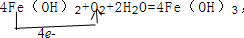 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
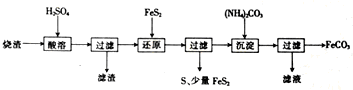
| 离子 | 离子浓度(mol?L-1) | |
| 还原前 | 还原后 | |
| Fe2+ | 0.10 | 2.50 |
| SO42- | 3.50 | 3.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
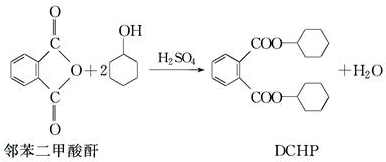
| A. | 邻苯二甲酸酐属于酸性氧化物 | |
| B. | 环己醇分子中所有的原子可能共平面 | |
| C. | DCHP能发生加成、取代、消去反应 | |
| D. | 1molDCHP最多可与含2molNaOH的烧碱溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com