
(14分)实验室用乙醇和浓硫酸反应制备乙烯,化学方程式为:C2H5OH CH2=CH2↑+H2O,接着再用液溴与乙烯反应制备1,2-二溴乙烷。在制备过程中由于部分乙醇与浓硫酸发生氧化还原反应还会产生CO2、SO2 ,并进而与Br2反应生成HBr等酸性气体。某学习小组用上述三种为原料,组装下列仪器(短接口或橡皮管均己略去)来制备1,2-二溴乙烷
CH2=CH2↑+H2O,接着再用液溴与乙烯反应制备1,2-二溴乙烷。在制备过程中由于部分乙醇与浓硫酸发生氧化还原反应还会产生CO2、SO2 ,并进而与Br2反应生成HBr等酸性气体。某学习小组用上述三种为原料,组装下列仪器(短接口或橡皮管均己略去)来制备1,2-二溴乙烷

(1)如果气体流向从左到右,正确的连接顺序是:
B经A①插入A中,D接入②;A③接 接 接 接 接。
(2)温度计水银球的正确位置是 。
(3)装置D与分流漏斗相比,其主要优点是 。
(4)装置C的主要作用是 ,装置F的作用是 。
(5)在反应管E中进行的主要反应的化学方程式为 。
(6)装置E烧杯中的泠水和反应管内液溴上的水层作用均是 。若将装置F拆除,在E中的主要反应为 。
(1)C、F、E、G(2分) (2)位于三颈瓶的液体中央(1分)
(3)平衡上下压强,使液体顺利滴下(2分)
(4)防倒吸(1分)除去三颈瓶中产生的CO2 、SO2 (2分)吸收挥发的溴蒸汽(1分)
(5)CH2=CH2 + Br2 BrCH2CH2Br(2分)
BrCH2CH2Br(2分)
(6)减少溴的挥发(1分);SO2+Br2+H2O=H2SO4+2HBr(2分)
【解析】
试题分析:(1)根据装置中试剂可知ABD用来制备乙烯,由于生成的乙烯中含有SO2和CO2等气体,在利用乙烯与溴反应之前需要除去。C起到安全瓶的作用,目的是为防止倒吸。E装置用来制备1,2—二溴乙烷,生成的1,2—二溴乙烷中含有溴,利用F装置除杂,最后利用G装置进行尾气处理,则正确的连接顺序是B经A①插入A中,D接入②;A③接C、F、E、G。
(2)温度计测量的是溶液的温度,因此位于三颈瓶的液体中央。
(3)D是恒压漏斗,能保持内外压强相同,则其作用是平衡上下压强,使液体顺利滴下。
(4)根据以上分析可知装置C的主要作用是防倒吸。装置F的作用是除去三颈瓶中产生的CO2、SO2吸收挥发的溴蒸汽。
(5)E装置用来制备1,2—二溴乙烷,反应的方程式为CH2=CH2 + Br2 BrCH2CH2Br。
BrCH2CH2Br。
(6)由于液溴易挥发,则装置E烧杯中的泠水和反应管内液溴上的水层作用均是减少溴的挥发;若将装置F拆除,则SO2易与溴发生氧化还原反应,所以在E中的主要反应为SO2+Br2+H2O=H2SO4+2HBr。
考点:考查有机物制备实验方案设计与探究


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源:2014-2015学年四川省资阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:推断题
(15分)已知: 。
。

醇酸树脂是一种成膜性良好的树脂,下面是一种醇酸树脂的合成线路:
(1)B中含碳官能团的结构式为_____,C的名称是_____。
(2)反应①的有机反应类型是_____。
(3)下列说法正确的是_____(填字母编号)。
a.1 mol E与足量的银氨溶液反应能生成2 mol Ag
b.F能与NaHCO3反应产生CO2
c.检验CH3CH2CH2Br中的溴原子时,所加试剂的顺序依次是过量氢氧化钠溶液、硝酸银溶液
(4)写出E与新制的氢氧化铜悬浊液反应的化学方程式_____;
(5)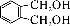 的同分异构体中同时符合下列条件的芳香族化合物共有_____种。
的同分异构体中同时符合下列条件的芳香族化合物共有_____种。
a.能发生消去反应 b.能与过量浓溴水反应生成白色沉淀
(6)写出反应⑤的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市静安区高三上学期期末考试化学试卷(解析版) 题型:选择题
与100 mL 0.1mol/L (NH4)2SO4溶液中c(NH4+)基本相同的是
A.200 mL 0.1 mol/L NH4Cl 溶液 B.50 mL 0.2 mol/L NH4NO3溶液
C.100 mL 0.2 mol/L NH4HSO4 D.50 mL 0.2 mol/L氨水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省安康市高三上学期第二次教学质量调研化学试卷(解析版) 题型:选择题
将气体R和SO2气体分别通入BaCl2溶液中,都未见沉淀生成;若同时通入两种气体会有沉淀生成,则气体R不可能为
A.CO2 B.NH3 C.Cl2 D.NO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省安康市高三上学期第二次教学质量调研化学试卷(解析版) 题型:选择题
某有机物的分子式为C8H8O2,含有苯环和-COOH的同分异构体有
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省晋中市高三1月考前适应性训练理综化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大,原子半径r(W)>r(Y)>r(Z)>r(X),X与W同主族,Z原子最外层电子数是其内层电子总数的3倍,Z原子的核电荷数等于X、Y原子核电荷数之和。下列说法正确的是
①工业上常用电解的方法制备W的单质
②化合物X2Z2与W2Z2所含化学键类型完全相同
③仅由X、Y、Z三种元素形成的化合物水溶液一定呈碱性
④元素Z的简单气态氢化物热稳定性比Y强
A.②④ B.①② C.①④ D.①③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省滕州市高三12月月考理综化学试卷(解析版) 题型:填空题
(16分)
某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可用于生产颜料铁红和补血剂乳酸亚铁。其生产工艺流程如下:

已知:①TiOSO4可溶于水,在水中可以电离为Ti02+和SO4 :
:
②TiOSO4水解的反应为:
请回答:
(1)步骤①所得滤渣的主要成分为______________________________。
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为__________________。
(3)步骤④需控制反应温度低于35℃,其目的是___________________。
(4)步骤④反应的离子方程式是__________________________________。
(5)已知: ,试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因_________________________________________________________。
,试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因_________________________________________________________。
(6)溶液B常被用于电解生产(NH4)2S208(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为_____________________________________。
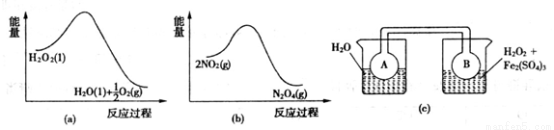
(7)Fe3+对H2O2的分解具有催化作用。利用下图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的_________(填“深”或“浅”),其原因是_________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省盐城市高二12月月考化学试卷(解析版) 题型:选择题
13.已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
A.加少量烧碱溶液 B.升高温度
C.加少量冰醋酸 D.加水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三“一诊”理综化学试卷(解析版) 题型:选择题
下列有关溶液中粒子浓度关系的比较中不正确的是
A.饱和氯水中滴加0.1 mol·L-1的NaOH溶液,溶液pH=7时:c(Na+)=2c(ClO-)+c(HClO)
B.已知HF的酸性比CH3 COOH的强,pH相等的NaF与CH3 COOK溶液中:c(Na+)-c(F-)=c(K+) -c(CH3COO-)
C.0.lmol/L pH为1的NaHB溶液中:c(Na+)>c(B2﹣)>c(H+)>c(OH﹣)
D.常温下,向20.00 mL 0.100 mol·L-1 NaA溶液中逐滴加入0.100 mol·L-1盐酸溶液的pH=7时:c(HA)=c(Cl-)>c(OH-)=c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com