
下列溶液中物质的量浓度为1mol/L的是( )
|
| A. | 将40g NaOH溶解在1L水中 |
|
| B. | 将22.4L HCl气体溶于水配成1L溶液 |
|
| C. | 从1L 2mol/L的H2SO4溶液中取出0.5L |
|
| D. | 将10g NaOH溶解在少量水中,再加蒸馏水至溶液体积为250mL |
考点:
物质的量浓度.
专题:
物质的量浓度和溶解度专题.
分析:
A、40 g NaOH为1mol,溶于水配成1L溶液,浓度为1mol/L,体积是溶液的体积,不是溶剂的体积;
B、HCl所处的状态不确定,22.4LHCl气体的物质的量不一定是1mol;
C、溶液的浓度与体积无关;
D、根据n= 计算氢氧化钠的物质的量,再根据c=
计算氢氧化钠的物质的量,再根据c=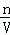 计算.
计算.
解答:
解:A、40 g NaOH为1mol,溶于水配成1L溶液,浓度为1mol/L,体积1L是溶液的体积,不是溶剂的体积,故A错误;
B、HCl所处的状态不确定,22.4LHCl气体的物质的量不一定是1mol,溶于水配成1L溶液,浓度不一定是1mol/L,故B错误;
C、溶液的浓度与体积无关,从1L 2mol/L的H2SO4溶液中取出0.5L溶液的浓度仍然为2mol/L,故C错误;
D、10g NaOH的物质的量为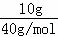 =0.25mol,溶液体积为250mL,故氢氧化钠溶液的浓度为
=0.25mol,溶液体积为250mL,故氢氧化钠溶液的浓度为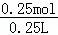 =1mol/L,故D正确;
=1mol/L,故D正确;
故选D.
点评:
本题考查学生对物质的量浓度的理解、常用化学计量的有关计算,难度不大,注意B选项为易错点,容易忽略气体摩尔体积的使用条件,注意对物质的量浓度定义式的理解.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
-A.-同种胶体带同种电荷,相互排斥,是胶体稳定的主要原因
-B.-生石灰与水混合的过程只发生物理变化
-C.-O3是由3个氧原子构成的化合物
-D.-可用丁达尔效应区分溶液与胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中物质的量浓度为1mol/L的是( )
|
| A. | 将40g NaOH溶解在1L水中 |
|
| B. | 将22.4L HCl气体溶于水配成1L溶液 |
|
| C. | 从1L 2mol/L的H2SO4溶液中取出0.5L |
|
| D. | 将10g NaOH溶解在少量水中,再加蒸馏水至溶液体积为250mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 摩尔是6.02×1023个结构微粒的集体 |
|
| B. | 0.012kg12C所含的原子数精确值是6.02×1023 |
|
| C. | 1molH就是1mol氢 |
|
| D. | 1molH2SO4的质量是98g |
查看答案和解析>>
科目:高中化学 来源: 题型:
配制250mL0.5mol/L的盐酸溶液,需4mol/L的盐酸的体积是( )
|
| A. | 25mL | B. | 31.3mL | C. | 12.5mL | D. | 100mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用NaOH固体配制480mL 1.0mol/L的NaOH溶液,请回答下列问题:
(1)应称取NaOH固体的质量 g
(2)实验仪器除了托盘天平、药匙、烧杯、玻璃棒外,还应有
(3)容量瓶上需标有以下五项中的 (序号)
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(4)使用容量瓶前必须进行的一步操作是 .
(5)配制时,其正确的操作顺序是
A、用30mL水洗涤烧杯2﹣3次,洗涤液均转入容量瓶,振荡
B、用托盘天平准确称取所需质量的NaOH,放入烧杯,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入500mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切
F、继续往容量瓶内小心加水,直到液面接近刻度线1﹣2cm处
(6)下列配制的溶液浓度偏大的是
A、NaOH在烧杯中溶解后,未冷却就转移到容量瓶中
B、向容量瓶中转移溶液时,不慎有液滴洒在容量瓶外面
C、未洗涤溶解NaOH的烧杯
D、定容时俯视刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同的下列溶液中,符合按pH由小到大的顺序排列的是()
A. Na2CO3NaHCO3NaClNH4Cl B. Na2CO3NaHCO3NH4ClNaCl
C. (NH4)2SO4NH4ClNaNO3Na2S D. NH4Cl(NH4)2SO4Na2SNaNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
电化学降解NO3﹣的原理如图所示,若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(△m左﹣△m右)为a克,则a值为()
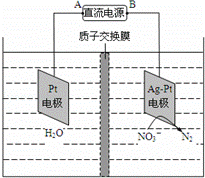
A. 14.4 B. 10.4 C. 12.4 D. 14.0
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)⇌2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表.下列说法正确的是()
t/min 2 4 7 9
n(Y)/mol 0.12 0.11 0.10 0.10
A. 反应前2min的平均速率v(Z)=2.0×10﹣5mol/(L•min)
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2mol Z,平衡时X的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com