
分析 由②C+NaOH→蓝色沉淀D+F可知,蓝色沉淀D为Cu(OH)2,
由④F+Ba(NO3)2→白色沉淀+NaNO3可知,白色沉淀为硫酸钡,则F为Na2SO4,
由③D$\stackrel{△}{→}$A+E、①A+B→C+E 可知,A为CuO,B为H2SO4,E为H2O,C为CuSO4,以此来解答.
解答 解:(1)由上述分析可知A为 CuO,B为H2SO4,C为 CuSO4,D为Cu(OH)2,E为 H2O,F为Na2SO4,
故答案为:CuO;H2SO4;CuSO4;Cu(OH)2;H2O;Na2SO4;
(2)离子反应方程式分别为①CuO+2H+=Cu2++H2O、②Cu2++2OH-=Cu(OH)2↓、④Ba2++SO42-=BaSO4↓,
故答案为:CuO+2H+=Cu2++H2O;Cu2++2OH-=Cu(OH)2↓;Ba2++SO42-=BaSO4↓.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应为解答的关键,蓝色沉淀及白色沉淀为推断的突破口,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度不大.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “尿毒症”患者做血液透析治疗 | |
| B. | FeCl3溶液中滴入NaOH溶液出现红褐色沉淀 | |
| C. | 在河流入海处易形成沙洲 | |
| D. | 在豆浆中加入盐卤制豆腐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
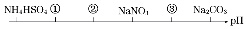 相同温度,相同浓度下的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分別为( )
相同温度,相同浓度下的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分別为( )| A. | NH4Cl、(NH4)2SO4、CH3COONa | B. | (NH4)2SO4、NH4Cl、CH3COONa | ||
| C. | (NH4)2SO4、NH4Cl、NaOH | D. | CH3COONa、NH4Cl、(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01 mol•L-1HA的溶液中 c(H+)=l×l0-4mol•L-1 | |
| B. | pH=3的HA溶液与pH=ll的NaOH溶液等体积混合后所得溶液中:c(Na+)=c(A-)>c(OH-)=c(H+) | |
| C. | 浓度均为0.1 mol•L-1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(H+)-c(OH-)>c(A-)-c(HA) | |
| D. | pH=3的HA溶液与pH=11的NaOH溶液混合后所得溶液显碱性,则 c(Na+)>c(A-)>c(OH-)><c(H+) |
查看答案和解析>>
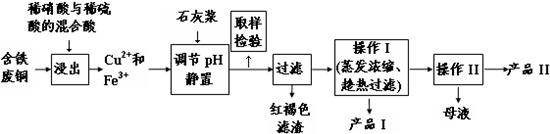
科目:高中化学 来源: 题型:解答题
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 在试管中加入少量FeCl3溶液和过量 (填少量、过量)的KI溶液. | 深红色如期出现 |
| ② | 将试管中的混合溶液转移至分液漏斗 (填仪器)中,倒入一定量的CCl4, 塞住活塞,充分振荡(萃取),静置. | 液体分层,上层接近无色,下层紫红色 |
| ③ | 打开活塞,先放出下层液体,再从分液漏斗的上口中倒出水层于试管中,加入KSCN溶液 | 出现血红色,则反应后的混合物中含Fe3+,进而证明这的确是一个可逆反应;反之则不含Fe3+,进而证明不是一个可逆反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com