
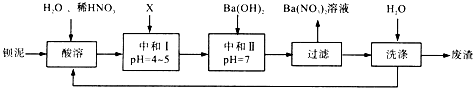
���� ������Ҫ��BaCO3��BaSO3��Ba��FeO2��2�ȣ��������ᣬ�������г���ܽ⣬���������ᱵ�����˺���Һ�к��������ӡ������ӵȣ�����Һ�����ԣ��ɼ���̼�ᱵ��������ҺpH=4��5��ʹ������ˮ������Fe��OH��3���������˺����ΪFe��OH��3����Һ�к������ᡢ���ᱵ�ȣ��������������к͵õ����ᱵ��Һ����������Ũ�������˿ɵõ����ᱵ���壬ĸҺ�к������ᱵ�����˵õ��Ĺ���ϴ�Ӻ��ȥ��������Һ���¼������ܲ��������ã�
��1����c��CO32-����c��Ba2+����Ksp��BaCO3��ʱ����ʵ�ֳ�����ת����
��2��Ba��FeO2��2��HNO3��Ӧ����Ba��NO3��2��Fe��NO3��3���Դ�ȷ����Ӧ�Ļ�ѧ����ʽ��
��3��X��Ҫ���������ᣬ�ֲ����������ʣ���ϱ���ʵ�ʣ��ʿ���BaCO3��
��4���к͢�ʹ��Һ�е�Fe3+����ˮ�������Fe��OH��3������
��5������Һ�еõ����壬Ӧ�������ᾧ�ķ�����
��6�����ݳ������ᱵ����������Ϸ���ʽ����������ᱵ��������������Ʒ�Ĵ��ȣ�
��� �⣺��1����Һ����BaSO4��aq��+CO32-��aq��?BaCO3��aq��+SO42-��aq������c��CO32-����c��Ba2+����Ksp��BaCO3��ʱ����ʵ�ֳ�����ת����
�ʴ�Ϊ��BaSO4��aq��+CO32-��aq��?BaCO3��aq��+SO42-��aq����
��2��Ba��FeO2��2���б�Ԫ��Ϊ+2�ۣ���Ԫ��Ϊ+3�ۣ����Է�Ӧ����ΪBa��NO3��2��Fe��NO3��3��
�����䷴Ӧ����ʽΪ��Ba��FeO2��2+8HNO3�TBa��NO3��2+2Fe��NO3��3+4H2O��
�ʴ�Ϊ��Ba��FeO2��2+8HNO3 =Ba��NO3��2+2Fe��NO3��3+4H2O��
��3��X��Ҫ���к����ᣬ�ֲ����������ʣ���Ϲ���ʵ�ʣ�Ӧ����BaCO3������pH���ʴ�Ϊ��B��
��4��Fe3+����ˮ�������Fe��OH��3���������ӷ���ʽΪFe3++3H2O?Fe��OH��3+3 H+������̼�ᱵ��BaCO3����H+ʹFe3+ˮ��ƽ�����ƣ��γ�Fe��OH��3������
�ʴ�Ϊ��ʹFe3+��ȫ������Fe3++3H2O?Fe��OH��3+3 H+��BaCO3����H+ʹFe3+ˮ��ƽ�����ƣ��γ�Fe��OH��3������
��5������Һ����ȡ���ʵķ���Ϊ������Ũ������ȴ�ᾧ��Ȼ����ˣ����Բ�����Ϊ����Ũ������ȴ�ᾧ���ʴ�Ϊ������Ũ������ȴ�ᾧ��
��6����ȡw�˾�����������ˮ���������������ᣬ��ַ�Ӧ���ˡ�ϴ�ӡ����������������Ϊm�ˣ��䷢���ķ�ӦΪ��Ba��NO3��2+H2SO4=BaSO4+2HNO3��
��μӷ�Ӧ��Ba��NO3��2Ϊxg��
Ba��NO3��2+H2SO4=BaSO4+2HNO3
261 233
x mg
�� $\frac{261}{x}=\frac{233}{mg}$�����x=$\frac{261m}{233}$�����Ը�Ba��NO3��2�Ĵ���Ϊ$\frac{\frac{261m}{233}}{w}$��100%=$\frac{261m}{233w}$��100%��
�ʴ�Ϊ��$\frac{261m}{233w}$��100%��
���� ���⿼��ѧ���ڡ����������Ķ�����ط�Ӧ��ѧ����ʽ��д����ѧ��Ӧ�������Ƶ�ԭ�����������̵����á��ȷ����Ԫ�ػ��������ʼ���ת����ϵ�������Ӧ�ó̶ȣ��ۺϿ���ѧ��������Ϣ�Ĵ�������������������ʵ����������Ŀ�Ѷ��еȣ�ע�����ʵ��ԭ���ͷ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ۢ� | B�� | �ڢۢ� | C�� | �ڢܢ� | D�� | �٢ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
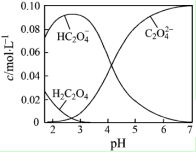 H2C2O4Ϊ��Ԫ���ᣮ20��ʱ������һ��c��H2C2O4��+c��HC2O4-��+c��C2O42-��=0.100mol•L-1��H2C2O4��NaOH�����Һ����Һ�в����������ʵ���Ũ����pH�ı仯������ͼ��ʾ������ָ����Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ���ǣ�������
H2C2O4Ϊ��Ԫ���ᣮ20��ʱ������һ��c��H2C2O4��+c��HC2O4-��+c��C2O42-��=0.100mol•L-1��H2C2O4��NaOH�����Һ����Һ�в����������ʵ���Ũ����pH�ı仯������ͼ��ʾ������ָ����Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ���ǣ�������| A�� | pH=2.5����Һ�У�c��H2C2O4��+c��C2O42-����c��HC2O4-�� | |
| B�� | c��Na+��=0.100 mol•L-1����Һ�У�c��H+��+c��H2C2O4��=c��OH-��+c��C2O42-�� | |
| C�� | c��HC2O4-��=c��C2O42-������Һ�У�c��Na+����0.100 mol•L-1+c��HC2O4-�� | |
| D�� | pH=7����Һ�У�c��Na+����2c��C2O42-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������������������һ����Ҫ���� | |
| B�� | һ����̼�����������������γɵ���Ҫ���� | |
| C�� | ��Ǧ�����ﵼ�����嵰���ʱ����������仯 | |
| D�� | ����β����ͨ������װ�ý�̼�⻯���ﻹԭ��CO2��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
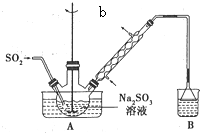 ���������Ƽ�ȩ��aNaHSO2•bHCHO•cH2O���׳Ƶ��飬�н�ǿ�Ļ�ԭ�ԣ��������±Ƚ��ȶ�����120�����Ϸֽ���������Σ���Na2SO3��SO2��HCHO��п��Ϊԭ�Ͽ��Ʊ����������Ƽ�ȩ��ʵ�鲽�����£�
���������Ƽ�ȩ��aNaHSO2•bHCHO•cH2O���׳Ƶ��飬�н�ǿ�Ļ�ԭ�ԣ��������±Ƚ��ȶ�����120�����Ϸֽ���������Σ���Na2SO3��SO2��HCHO��п��Ϊԭ�Ͽ��Ʊ����������Ƽ�ȩ��ʵ�鲽�����£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Al | P | S | Cl |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������������������ˮ�ŷŵ��콭�� | |
| B�� | �콭�ذ����ÿ�����ֽ������Ⱦ��ҵ | |
| C�� | ����Ͷ��ˮ�������Ż��콭��̬ | |
| D�� | ʹ�ú���ϴ�Ӽ��ҽ�ϴ�Ӻ�ķ�ˮ�ŷŵ��콭�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 13.8g | B�� | 69g | C�� | 34.5g | D�� | 138g |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com