二氧化碳碳捕获与封存技术(CCS)可以减少化石燃料燃烧以及其他工业用途的二氧化碳排放量,从而有助于减少温室气体的排放.该技术引起了各国的普遍重视.
Ⅰ.目前工业上有一种方法是用CO
2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO
2和3molH
2,一定条件下发生反应:
CO
2(g)+3H
2(g)?CH
3OH(g)+H
2O(g)△H=-49.0kJ/mol测得CO
2和CH
3OH(g)的浓度随时间变化如图1所示.
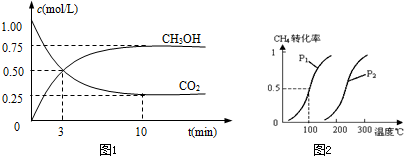
①从反应开始到平衡,氢气的平均反应速率v(H
2)=
0.225
0.225
mol/(L?min).
②下列措施中能使n(CH
3OH)/n(CO
2)增大的是
CD
CD
.
A.升高温度 B.充入He(g),使体系压强增大
C.将H
2O(g)从体系中分离 D.再充入1mol CO
2和3molH
2.
Ⅱ.工业上也可以通过下列反应①和②,用CH
4和H
2O为原料来制备甲醇.
①CH
4(g)+H
2O(g)?CO(g)+3H
2(g)△H1;②CO(g)+2H
2(g)?CH
3OH(g)△H
2将0.20mol CH
4和0.30molH
2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH
4的转化率与温度、压强的关系如图2.
(1)温度不变,缩小体积,增大压强,①的反应速率
增大
增大
(填“增大”、“减小”或“不变”),平衡向
逆反应
逆反应
方向移动.
(2)反应①的△H
1>
>
0(填“<”、“=”或“>”),其平衡常数表达式为K=
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
,压强为P
1,100℃时的平衡常数值是
1.35×10-3
1.35×10-3
.



