
 A~H是中学化学常见的物质,它们之间的转化关系如图所示(部分产物已略去).已知B、D是生活中常见的金属单质,G是气体单质,C的焰色反应呈黄色.
A~H是中学化学常见的物质,它们之间的转化关系如图所示(部分产物已略去).已知B、D是生活中常见的金属单质,G是气体单质,C的焰色反应呈黄色.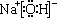 ,H为H2O,结构式为H-O-H,
,H为H2O,结构式为H-O-H,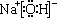 ;H-O-H;
;H-O-H;
| ||
| ||


科目:高中化学 来源: 题型:
| A、标准状况下,2.24L甲醇中含有的分子数为0.1NA |
| B、1L 0.1mol/L Na2CO3溶液中,含有的CO32-数目为0.1NA |
| C、室温下,1.40g乙烯和丁烯的混合气体中含有的碳原子数目为0.1NA |
| D、标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Na+、Fe2+、Cl-、SO
| ||||||
B、K+、Na+、[Al(OH)4]-、NO
| ||||||
C、Ba2+、Na+、NO
| ||||||
D、NH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molNH4+中含有10NA个质子 |
| B、t℃时,1LpH=6的纯水中,含1×10-6 NA个OH- |
| C、78gNa2O2中含阴离子的数目为2 NA |
| D、向FeI2溶液中通入适量氯气,当有1molFe2+被氧化时,总共转移电子的数目为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,62g白磷分子中的共价键数为3NA |
| B、标准状况下,2.24L NH3和CH4的混合气体,所含电子总数为2NA |
| C、58.5g NaCl晶体中所含的氯化钠分子数目为NA |
| D、Na2O2与H2O反应生成11.2L O2(标准状况),反应中转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 L 1 mol?L-1的FeCl3溶液中含有NA个Fe3+ |
| B、往某容器中投入1molN2和3molH2,一定条件下充分反应后,生成的NH3的数目为2NA |
| C、钠与水反应生成1.12LH2,反应中转移的电子数为0.1NA |
| D、常温常压下,22g氧气和26g臭氧混合气体所含氧原子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol Cl2参加化学反应获得的电子数都是2NA |
| B、1mol CnH2n+2含有(3n+1)NA个共价键 |
| C、标准状况下,11.2L NO与11.2L O2混合后所含原子数为2NA |
| D、电解精炼铜时,电解池中每转移1mol电子,阳极上溶解的铜原子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl2和KSCN |
| B、AgNO3和HNO3 |
| C、KMnO4和H2SO4 |
| D、KI和淀粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com