
下图所示的实验,能达到实验目的是()
A. 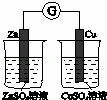
验证化学能转化为电能 B. 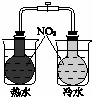
证明温度对平衡移动的影响
C. 
验证铁发生析氢腐蚀 D. 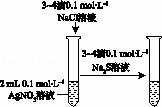 验证AgCl溶解度大于Ag2S
验证AgCl溶解度大于Ag2S
考点: 化学实验方案的评价.
专题: 化学实验基本操作.
分析: A.缺少盐桥;
B.根据2NO2⇌N2O4的平衡移动判断;
C.发生吸氧腐蚀;
D.银离子过量,不能证明.
解答: 解:A.没有形成闭合回路,缺少盐桥,故A错误;
B.温度改变,根据颜色变化可知2NO2⇌N2O4的平衡移动,故B正确;
C.在中性条件下铁发生吸氧腐蚀,故C错误;
D.银离子过量,不能证明,故D错误.
故选B.
点评: 本题考查化学实验方案的评价,涉及原电池的设计、化学平衡的影响因素、金属的腐蚀以及难溶电解质的溶解平衡,为2015届高考常见题型,综合考查学生的实验评价和分析能力,题目难度不大,注意把握相关物质的性质.


科目:高中化学 来源: 题型:
所含分子数相同的一组物质是( )
|
| A. | 1gH2和1gN2 | B. | 1molH2O和1gH2O |
|
| C. | 3.2gO2和4.8gO3 | D. | 44gCO2和16gO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在20g密度为d g/cm3的硝酸钙溶液里含1g Ca2+,则硝酸根离子的物质的量浓度是( )
|
| A. |
| B. |
|
|
| C. | 1.25d mol•L﹣1 | D. | 2.5d mol•L﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状态下,气态分子断开1mol化学键的焓变为键焓.已知H﹣H,H﹣O和O=O键的键焓△H分别为436kJ•mol﹣1、463kJ•mol﹣1和495kJ•mol﹣1.下列热化学方程式正确的是()
A. H2O(g)═H2(g)+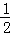 O2(g)△H=﹣485kJ•mol﹣1
O2(g)△H=﹣485kJ•mol﹣1
B. H2O(g)═H2(g)+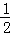 O2(g)△H=+485kJ•mol﹣1
O2(g)△H=+485kJ•mol﹣1
C. 2H2(g)+O2(g)═2H2O(g)△H=+485kJ•mol﹣1
D. 2H2(g)+O2(g)═2H2O(g)△H=﹣485kJ•mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中粒子的物质的量浓度关系正确的是()
A. 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32﹣)>c(HCO3﹣)>c(OH﹣)
B. 20mL 0.1mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO﹣)>c(Cl﹣)>c(CH3COOH)>c(H+)
C. 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl﹣)+c(H+)>c(NH4+)+c(OH﹣)
D. 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH﹣)>c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)NH3经一系列反应可以得到HNO3和NH4NO3,如图所示,在Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是 .
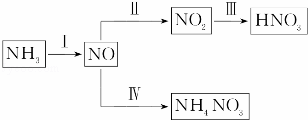
(2)Ⅱ中,2NO(g)+O2(g)⇌2NO2(g).在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图).
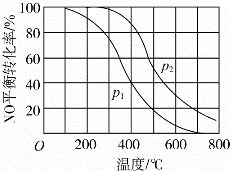
①p1、p2的大小关系 .
②随温度升高,该反应平衡常数变化的趋势是
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(1)再制备浓硝酸.
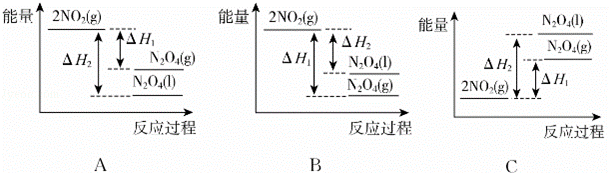
①已知:2NO2(g)⇌N2O4(g)△H1 2NO2(g)⇌N2O4(1)△H2
下列能量变化示意图3中,正确的是A(选填字母)
②N2O4与O2,H2O化合的化学方程式是
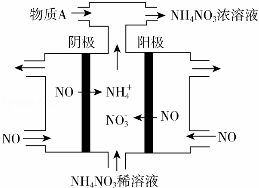
(4)Ⅳ中,电解NO制备NH4NO3,其原理原理如图4所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是NH3,说明理由: .
查看答案和解析>>
科目:高中化学 来源: 题型:
分别由氕(1H)、氘(2H)、氚(3H)组成的单质(均为双原子分子),其质量均为1g,则它们:
(1)原子个数比为 .
(2)电子个数比为 .
(3)相同条件下的密度之比为 .
(4)相同条件下的体积之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,一定浓度的某溶液,由水电离出的c(OH﹣﹣)=10﹣﹣4mol/L,则该溶液中的溶质可能是()
A. Na2SO4 B. CH3COOH C. NaOH D. CH3COOK
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com