
| A. | 发生装置与氯酸钾制取氧气相同 | |
| B. | 可以用碱石灰干燥氨气 | |
| C. | 棉花的作用和高锰酸钾制取氧气一样 | |
| D. | 氨气验满的方法是将湿润的红色石蕊试纸放于集气瓶附近 |
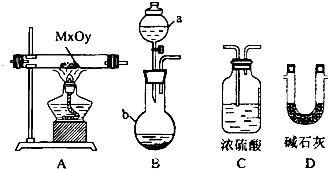
分析 A.依据反应物状态和反应条件选择发生装置;
B.氨气为碱性气体,应选择碱性干燥剂;
C.制备氨气试管口塞棉花是为防止与空气形成对流;
D.氨气与水反应生成一水合氨,一水合氨电离产生氢氧根离子,显碱性;
解答 解:A.氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,氯化铵与氢氧化钙固体在加热条件下生成氨气,反应物状态都是固体与固体,反应条件都是加热,所以二者发生装置相同,故A正确;
B.氨气为碱性气体,应选择碱性干燥剂,碱石灰为碱性干燥剂,可以干燥氨气,故B正确;
C.制备氨气试管口塞棉花是为防止与空气形成对流,高锰酸钾制备氧气,导管口塞棉花,防止固体颗粒堵塞导气管发生爆炸,二者作用不同,故C错误;
D.氨气与水反应生成一水合氨,一水合氨电离产生氢氧根离子,显碱性,将湿润的红色石蕊试纸放于集气瓶附近,若变蓝说明收集满,故D正确;
故选:C.
点评 本题考查了氨气的性质和检验方法,明确氨气性质是解题关键,注意氨气的检验可以用湿润的红色石蕊试纸,也可用沾有浓盐酸的玻璃棒.


科目:高中化学 来源: 题型:解答题
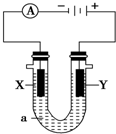 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学兴趣小组为了测定某草酸晶体的纯度及硫酸酸化的高锰酸钾溶液与草酸(H2C2O4)溶液反应的化学反应速率大小的影响因素,设计了如下实验.化学反应如下:
某化学兴趣小组为了测定某草酸晶体的纯度及硫酸酸化的高锰酸钾溶液与草酸(H2C2O4)溶液反应的化学反应速率大小的影响因素,设计了如下实验.化学反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 固体成分(填化学式) |
| 1 | |
| 2 | |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{O}_{3}^{-})}$=$\frac{1}{2}$ | |
| B. | 参加反应的氯气的物质的量等于$\frac{1}{2}$ a mol | |
| C. | 改变温度,反应中转移电子的物质的量ne的范围:$\frac{1}{2}$ a mol≤ne≤$\frac{5}{6}$ a mol | |
| D. | 改变温度,产物中KClO3的最大理论产量为$\frac{1}{7}$a mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
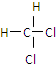 和
和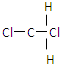
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A和B不可能是同系物 | |
| B. | A和B一定是同分异构体 | |
| C. | A和B最简式一定相同 | |
| D. | 等物质的量的A和B完全燃烧生成等质量的CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯硝酸钾晶体 | B. | 大量硝酸钾晶体,少量氯化钠 | ||
| C. | 等量的硝酸钾和氯化钠 | D. | 大量氯化钠,少量硝酸钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂,可以加快反应速率 | |
| B. | 可逆反应A(g)?B(g)+C(g),增大压强正反应速率和逆反应速率增大 | |
| C. | 对达到平衡的一个放热的可逆反应,若降低温度正反应速率减小,逆反应速率增大 | |
| D. | 参加反应物质的性质是决定化学反应速率的主要因素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com