
����Ŀ��A��B��C��D��E��ǰ������ԭ�������������������Ԫ�ء�AԪ��ԭ�ӵĺ����������������Ӳ�����BԪ�ػ�̬ԭ���������ܼ��Ҹ��ܼ���������ͬ�� A��D���γ����ֳ���Һ̬������G��H����ԭ����֮�ȷֱ�Ϊ1:1��2:1��EԪ��ԭ�ӵ�K��L�������֮�͵�����M��N�������֮�͡���ش����и��⣨�漰Ԫ��������Ӧ��ѧ���ű�ʾ����
��1�� B��C��D����Ԫ���е縺������Ԫ�����̬ԭ�ӵĵ����Ų�ͼΪ ��
��2������һ���ռ��˶�״̬�ĵ�����ԭ�Ӻ�����ֵĸ����ܶȷֲ����� ������������B�Ļ�̬ԭ���У�������� �������෴�ĵ��ӡ�
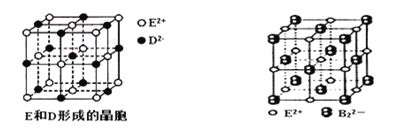
��3����E��D�γɵľ�����ͼ1��ʾ��������E2+��Χ�Ⱦ��������E2+��________����ED����ɫ��ӦΪש��ɫ��������������ǵĻ����ﶼ���Է�����ɫ��Ӧ����ԭ���� ��E��B���γɵľ���ľ����ṹ��NaCl��������ƣ���ͼ2��ʾ�������þ����к��е�������B22���Ĵ��ڣ�ʹ������һ������������������E2+����λ��Ϊ______���û�����ĵ���ʽΪ ��
��4���ø�����������Һ̬Hʱ��һ��H�������ͷų�һ�����ӣ�ͬʱ����һ�������ӡ�
���ͷų����ĵ��ӿ��Ա�����H�����γɵ���������������ΪH���Ӽ����γ���������ԭ���� ��
����H�����ͷų�һ������ʱ������һ�������Ӿ��н�ǿ�������ԣ���д������������SO2��ˮ��Һ��Ӧ�����ӷ���ʽ ��
���𰸡���1�� 1s22s22p4
��2�� ������ 2
��3�� 12�� ��̬ԭ�ӵĵ��ӷ���ԾǨ���������֣� 6![]() ��
��
��4����ˮ���Ӽ������� ��2H2O++SO2��SO42��+4H+
�����������������A��B��C��D��E��ǰ������ԭ�������������������Ԫ�ء�AԪ��ԭ�ӵĺ����������������Ӳ�������AΪHԪ�أ�BԪ�ػ�̬ԭ���������ܼ��Ҹ��ܼ���������ͬ����������Ų�ʽΪ1s22s22p2����BΪ̼Ԫ�أ�A��D���γ����ֳ���Һ̬������G��H����ԭ����֮�ȷֱ�Ϊ1��1��2��1����DΪOԪ�ء�GΪH2O2��HΪH2O��C��ԭ����������̼����֮�䣬��CΪNԪ�أ�EԪ��ԭ�ӵ�K��L�������֮�͵�����M��N�������֮�ͣ�ԭ�Ӻ��������Ϊ��2+8����2��20����EΪCa��
��1��ͬ����������ҵ縺������C��N��O�е縺������Ԫ��ΪOԪ�أ����̬ԭ�Ӻ�������Ų�ʽΪ1s22s22p4��
��2������һ���ռ��˶�״̬�ĵ�����ԭ�Ӻ�����ֵĸ����ܶȷֲ����õ���������������BΪ̼Ԫ�أ���̬ԭ�Ӻ�������Ų�ʽΪ1s22s22p2���������2�������෴�ĵ��ӣ�
��3��ij�����ᄃ���ṹ��ͼ��ʾ���Զ����E2+�о�����֮�Ⱦ��������E2+λ�����ģ�ÿ������Ϊ8���������ã�ÿ������Ϊ2���������ã��ʾ�����E2+��Χ�Ⱦ��������E2+��![]() ����ED����ɫ��ӦΪש��ɫ��������������ǵĻ����ﶼ���Է�����ɫ��Ӧ����ԭ���ǣ�����̬�ĵ���ԾǨ�����ܼ�ʱ���Թ����ʽ�ͷ�������E��B���γɵľ���ľ����ṹ��NaCl��������ƣ����þ����к��е�������B22-�Ĵ��ڣ�ʹ������һ������������������E2+����λ��Ϊ6���û�����ΪCaC2��̼����Ϊ���ӻ��������ʽΪ
����ED����ɫ��ӦΪש��ɫ��������������ǵĻ����ﶼ���Է�����ɫ��Ӧ����ԭ���ǣ�����̬�ĵ���ԾǨ�����ܼ�ʱ���Թ����ʽ�ͷ�������E��B���γɵľ���ľ����ṹ��NaCl��������ƣ����þ����к��е�������B22-�Ĵ��ڣ�ʹ������һ������������������E2+����λ��Ϊ6���û�����ΪCaC2��̼����Ϊ���ӻ��������ʽΪ![]() ��
��
��4���ø�����������Һ̬ˮʱ��һ��ˮ�������ͷų�һ�����ӣ�ͬʱ����һ��������ΪH2O+����
��ˮ���Ӽ����γ���������ԭ���ǣ�ˮ���Ӽ���������
����H�����ͷų�����ʱ������һ�������Ӿ��н�ǿ�������ԣ�����������SO2ˮ��Һ��Ӧ���ӷ���ʽΪ2H2O++SO2��SO42��+4H+��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��R��ԭ��������������Ķ���������Ԫ�أ�X�����ڱ���ԭ�Ӱ뾶��С��Y��Z���ڣ�Z��R�ڵؿ��еĺ���λ��ǰ��λ��MΪ�������е縺����С��Ԫ�ء���ش�
��1����̬Zԭ�ӵ���Χ�����Ų�ͼΪ____________��
��2��X��Y���γɶ��ֻ��������Y2X2�����ЦҼ����м�����Ŀ֮��Ϊ_______��
��3����R3Y4�����м��ǣ�Y-R-Y____R-Y-R���>����<����=������ԭ��Ϊ________��
��4���٣�W��Ԫ�ؿ��Ժ�Z��M�γɶ��ֻ��������һ�ֻ�����ľ���ṹ��ͼ��

��֪������Zԭ�ӵĺ˼��Ϊapm����ԭ��λ��Zԭ���γɵ�������������ģ�M����λ����ԭ���γɵ�����������ġ�
����Mԭ�Ӿ����������ȵ�Zԭ�ӵ���ĿΪ_________��
�ھ���Ļ�ѧʽΪ__________��
����NAΪ�����ӵ�������ֵ��������ܶ�Ϊ______g/cm3���г�����ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭƬ����ʢ������ϡ������ձ��У���ʹͭƬ�ܽ⣬�������ձ��м���
A. ���Ȼ������� B. ����粒���
C. ϡ������Һ D. ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ԷϾ�Ǧ�����еĺ�Ǧ���ϣ�Pb��PbO��PbO2��PbSO4��̿�ڵȣ�Ϊԭ�ϣ��Ʊ���Ǧ��ʵ��Ǧ���������á��乤����������ͼ��ʾ��
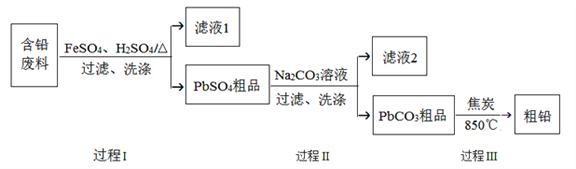
��֪��Ksp(PbSO4)=1.6��10-5,Ksp(PbCO3)=3.3��10-14.
��1�����̢��У���Fe2+���£�Pb��PbO2��Ӧ����PbSO4�Ļ�ѧ����ʽ��__________��
��2�����̢��У�Fe2+�����̿ɱ�ʾΪ��
i��2Fe2++ PbO2+4H++SO42-![]() 2Fe3++PbSO4+2H2O
2Fe3++PbSO4+2H2O
ii: ����
��д��ii�����ӷ���ʽ��________________��
������ʵ�鷽����֤ʵ���������̡���ʵ�鷽������������
a.���ữ��FeSO4��Һ�м���KSCN��Һ����Һ������ɫ���ټ�������PbO2����Һ��졣
b.___________��
��3�����̢��Ŀ������������Һ2��c(SO42-)=1.6mol/L,c(CO32-)=0.1mol/L,��PbCO3��____����ǡ�������PbSO4��
��4�������ӽ���Ĥ�����ⷨ�ǴӺ�Ǧ��������ȡǦ��һ���¹��գ���װ����ͼ��ʾ������Ǧ����Ͷ�������ң���Ǧ�����е�PbSO4��NaOH��Һ�� ����Ӧ:PbSO4+3OH-=HPbO2-+SO42-+H2O��
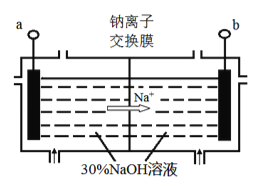
��a����ӵ�Դ��________��������
�ڵ������У�PbO2��PbO��HPbO2-�������ŵ磬����PbO2�ŵ�ĵ缫��ӦʽΪ___________��
���봫ͳ��Ĥ�����ⷨ��ȣ�ʹ�������ӽ���Ĥ���� ���PbԪ�ص������ʣ�ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڸ�������������ʴ�ķ�����ȷ����
A. ������ʴ�����ȷ�Ӧ B. ����ԭ�������
C. �����缫��ӦΪ��2H2O+O2+4e-=4OH- D. ԭ��ظ�����ӦΪ��Fe-3e-=Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���в���ȷ���ǣ� ��
A. ʯ�͵IJ����Ǻ���һ�����һ�ѧ��ҵˮƽ�ı�־
B. ʯ���ѻ�����������Ͳ���������������͵�����
C. ʯ�͵��ѽ���ѻ����ǻ�ѧ�仯�������ߵ�Ŀ�IJ�һ��
D. �������ѽ�����мȿɷ��������ѽ��ֿɷ��������ѽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W��R����ǰ������Ԫ�أ�ԭ������������������Xԭ��̬ʱ���������������ڲ����������2����Zԭ�ӻ�̬ʱs��������p��������ȣ�Z2-��W+����ͬ�ĺ�������Ų���R��ԭ������Ϊ29���ش��������⣺
��1��Y��Z��W����Ԫ�صĵ�һ��������С�����˳��Ϊ______����Ԫ�ط��ű�ʾ����
��2����M������Y2Z�ĵȵ����壬M�ĽṹʽΪ______, M���ӵ�����ԭ�ӵĹ���ӻ�����Ϊ________, 1molM�к���_____mol������
��3��Y�ļ��⻯�K������Z�ļ��⻯���У�����Ҫԭ����_____________��
��4����̬R+���ӵĺ�������Ų�ʽ��__________��R�ĸ�������Y������⻯���γɵ������ӵĻ�ѧʽΪ________________��
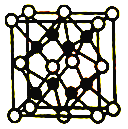
��5��Z��W�γɵĻ�����W2Z�ľ�����ͼ������Z���ӵ���λ��Ϊ________,��һ��Z���Ӿ������������W����Ϊ���㹹�ɵļ�����Ϊ________�ṹ����W2Z�ľ����߳�Ϊa pm����û�������ܶ�Ϊ_______g��cm-3���г�����ʽ���ɣ�����٤��������NA��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ϢϢ��أ������й�˵����ȷ����
A. �����м����Ȼ�����������ȱ����ƶѪ
B. ��ѩ��ҵ�δ�ຬ��NaCl����˿����ʳ��ʳ��
C. ʳ���͵���Ҫ�ɷ�����֬����ɷ������͡�ú����ͬ
D. ������ʰ�š���������������ʳ��ɱ�����������д���Ч�ɷ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��W��X��Y��Z��ԭ�������������ӡ�p��q��r������ЩԪ����ɵĶ�Ԫ�����m��n�ֱ���Ԫ��Y��Z�ĵ��ʣ�nͨ��Ϊ�����ɫҺ�壬0.01 mol/L r��Һ��pHΪ2��p��Ӣ����ѧ�ҷ����ڳ�Ϊ�������̼�������sͨ����������ˮ����ˮ�ص���״Һ�塣�������ʵ�ת����ϵ��ͼ��ʾ������˵������ȷ���ǣ� ��
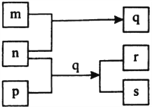
A. ԭ�Ӱ뾶�Ĵ�СW��X��Z
B. W�������ﳣ�³�ѹ��ΪҺ̬
C. Y����������ܳʺ�ɫ�����ɫ
D. Z���������ˮ����һ��Ϊǿ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com