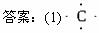【答案】
分析:G为黄绿色单质气体,所以G为Cl
2;
C通常状况下为无色液体,与Cl
2生成H和I,I有漂白作用,所以C为H
2O,H为HCl,I为HClO;
HCl与金属J反应得到K,为淡绿色溶液,所以J为Fe,K为FeCl
2,FeCl
2与Cl
2反应生成L,L为FeCl
3;
E为蓝色絮状沉淀,则E为Cu(OH)
2,FeCl
3与金属M反应到B,B再与NaOH溶液反应到达Cu(OH)
2沉淀,所以M为Cu,B为CuCl
2;
在周期表中X的原子半径最小,X为H元素,C、D是由X、Y、Z中两种元素组成的化合物,C为H
2O,所以Y、Z中两种元素有一种是O元素,Y、Z原子最外层电子数之和为10.所以另外元素的原子最外层电子数为4,D为无色非可燃性气体,所以D为CO
2,由于X、Y、Z三元素的原子序数依次增大,故Y为C元素、Z为O元素.
(1)A与HCl反应生成CuCl
2、H
2O、CO
2,所以A为Cu
2(OH)
2CO
3或CuCO
3;根据电子式、结构式书写写出C的电子式,D的结构式;
(2)同周期原子序数越大,原子半径越小;
(3)氯气氧化亚铁离子为铁离子,自身被还原为氯离子;
(4)根据现象及氧化还原反应书写;
(5)晶莹透明的晶体N,为碳单质,且为正四面体,故为金刚石,其同素异形体有石墨,富勒烯(C
60).
解答:解:G为黄绿色单质气体,所以G为Cl
2;
C通常状况下为无色液体,与Cl
2生成H和I,I有漂白作用,所以C为H
2O,H为HCl,I为HClO;
HCl与金属J反应得到K,为淡绿色溶液,所以J为Fe,K为FeCl
2,FeCl
2与Cl
2反应生成L,L为FeCl
3;
E为蓝色絮状沉淀,则E为Cu(OH)
2,FeCl
3与金属M反应到B,B再与NaOH溶液反应到达Cu(OH)
2沉淀,所以M为Cu,B为CuCl
2;
在周期表中X的原子半径最小,X为H元素,C、D是由X、Y、Z中两种元素组成的化合物,C为H
2O,所以Y、Z中两种元素有一种是O元素,Y、Z原子最外层电子数之和为10.所以另外元素的原子最外层电子数为4,D为无色非可燃性气体,所以D为CO
2,由于X、Y、Z三元素的原子序数依次增大,故Y为O元素、Z为C元素.
(1)A与HCl反应生成CuCl
2、H
2O、CO
2,所以A为Cu
2(OH)
2CO
3或CuCO
3,C为H
2O,其电子式为
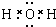
,D为CO
2,其结构式为O=C=O,
故答案为:Cu
2(OH)
2CO
3或CuCO
3;
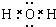
;O=C=O;
(2)Y为C元素、Z为O元素,同周期原子序数越大,原子半径越小,所以原子半径C>O,故答案为:C;O;
(3)氯气氧化亚铁离子为铁离子,自身被还原为氯离子,离子方程式为2Fe
2++Cl
2═2Fe
3++2Cl
-,故答案为:2Fe
2++Cl
2═2Fe
3++2Cl
-;
(4)Cu溶于稀硝酸,溶液变成蓝色,并放出无色气体,说明生成Cu
2+、NO等,反应方程式为3Cu+8HNO
3=3Cu(NO
3)
2+2NO↑+4H
2O,
故答案为:3Cu+8HNO
3=3Cu(NO
3)
2+2NO↑+4H
2O;
(5)晶莹透明的晶体N,为碳单质,且为正四面体,故为金刚石,其同素异形体有石墨,富勒烯(C
60),
故答案为:金刚石;石墨;富勒烯(C
60).
点评:本题以物质推断为载体,考查元素及其化合物的性质、化学用语等,综合性较大,难度中等,要掌握常见元素及其单质和化合物的性质.


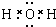 ,D为CO2,其结构式为O=C=O,
,D为CO2,其结构式为O=C=O,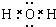 ;O=C=O;
;O=C=O;