
【题目】某小组为研究电化学原理,设计如图装置.下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C. 无论a和b是否连接,铁片均会溶解
D. a和b用导线连接后,Fe片上发生还原反应,溶液中的Cu2+向铜电极移动
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素 X、Y、Z 的单质 m、n、p 在通常状况下均为气态双原子分子,其中 m 含共用电子对数最多;甲、乙分别为 10 电子、18 电子分子,它们的转化关系如下图所 示(反应条件略去)。下列说法正确的是
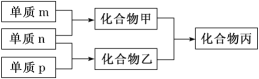
A. X 是同周期中非金属性最强的元素
B. 元素 X、Y、Z 的原子半径大小关系为 X<Y<Z
C. Z 的氧化物对应的水化物的酸性在主族元素中最强
D. 化合物丙是离子化合物,既含离子键又含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)某有机物(含C、H、O三种元素)分子球棍模型如图所示,下列有关叙述正确的是
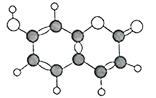
A. 分子式为C9H6O3
B. 不能使酸性KMnO4溶液褪色
C. 最多能与含1molNaOH的溶液反应
D. 能与碳酸氢钠溶液反应放出CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是

A. 离子半径: X>Y>Z
B. WX3和水反应形成的化合物是离子化合物
C. 最高价氧化物对应的水化物酸性:R>W
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程发生放热反应的是( )
A.固体NaOH溶于乙醇中 B.固体NH4Cl与Ba(OH)2混合
C.浓H2SO4加入水中 D.生石灰加入水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某磁黄铁矿的主要成分是FexS(S为-2价),既含有Fe2+,又含有Fe3+,将一定量的该磁黄铁矿与100mL的盐酸恰好完全反应(注:矿石中其他成分不与盐酸反应),生成2.4g硫单质,0.425mol FeCl2 和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是
A. 该盐酸的物质的量浓度为4.25mol·L-1
B. 该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3∶1
C. 成的H2S气体在标准状况下的体积为2.24L
D. 该磁黄铁矿中FexS的x=0.85
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废水中可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2-、CO32-、S2-、SO32-、SO42-。现取该溶液进行有关实验,实验过程及现象如下:

下列说法正确的是
A. 根据实验①中的现象可推出,气体A一定是纯净物,淡黄色沉淀A一定是AgBr
B. 根据实验②中现象可推出气体B是CO2,沉淀B是Al(OH)3,原溶液中一定含有Al3+
C. 根据实验③中的现象可推出,气体C是NH3,沉淀C一定含有BaCO3,可能含有BaSO4
D. 原溶液中肯定含有Na+、AlO2-、S2-,不能确定是否含有SO32-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在这些元素中,金属性最强的元素是_______,最活泼的非金属元素是_______;
(2)化学性质最不活泼的元素是__________,其原子的原子结构示意图为_____________;
(3)元素的最高价氧化物对应的水化物中酸性最强的是______________,碱性最强的是____________,呈两性的氢氧化物是____________________;
(4)③~⑦元素中,原子半径最大的是________,原子半径最小的是____________;
(5)在⑦与⑩的单质中,化学性质较活泼的是_____________,可用什么化学反应说明该事实(写出反应的化学方程式)____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铋酸钠(NaBiNO3)检验溶液中的Mn2+,反应方程式为:4MnSO4+10NaBiO3+14H2SO4═4NaMnO4+5Bi2(SO4)3+3Na2SO4+口,下列说法不正确的是
A. 口内的物质为水,配平系数为14。
B. 若生成1mol NaMnO4,则转移5mole-
C. 反应方程式中的硫酸可换为盐酸
D. 溶液中有Mn2+的现象是溶液变为紫红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com