
| A. | 20% | B. | 33.3% | C. | 50% | D. | 75% |
分析 设丙烷体积为YL,其中有X L的丙烷分解,依据丙烷分解方程式,列出三段式,依据碳原子个数守恒及燃烧得到二氧化碳关系计算解答.
解答 解:设共有C3H8 Y L,其中有X L的C3H8分解,
C3H8→CH4 +C2H4
起始时 Y 0 0
转化量 X X X
终止时 Y-X X X
分解后气体共1L,即Y-X+X+X=1,X+Y=1,故Y=1-X
分解后气体1L中 有 Y-X=1-2X L的C3H8 X L的CH4 XL的C2H4
依据碳原子守恒可知:1-2X L的C3H8生成的CO2有 3(1-2X),
CH4生成的CO2有 XL,
C2H4生成的CO2有 2X L
所以:3-6X+2X+X=2.25
解得X=0.25,所以原来丙烷有1-2X+X=0.75L,分解的丙烷就是0.25升,
丙烷的分解率就是$\frac{0.25}{0.75}$×100%=33.3%;
故选B.
点评 本题考查了有关方程式的计算,明确丙烷分解的方程式结合碳原子个数守恒即可解答,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
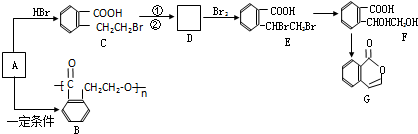
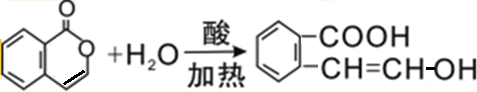
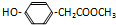 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 浓H2SO4和NaCl晶体 | B. | 甲酸和浓H2SO4(制CO) | ||
| C. | MnO2和浓硫酸 | D. | 浓H3PO4和NaBr晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH | B. | Na2CO3 | C. | Na2CO3、NaHCO3 | D. | NaOH、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
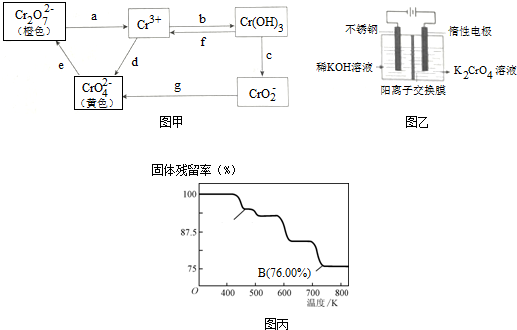
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | 最外层电子数是电子层数的2倍,单质为黑色固体 |
| B | 单质是空气的主要成分之一 |
| C | 与B不同主族,单质为淡黄色固体,易溶于二硫化碳 |
| D | 一种非金属元素 |
| E | 与D形成的某种化合物的水溶液遇苯酚溶液显紫色 |
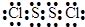
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
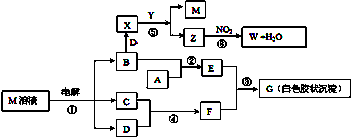
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
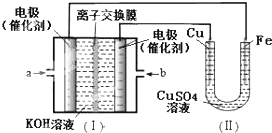
| A. | a处通入O2 | B. | b处发生氧化反应 | ||
| C. | 电流由Cu电极移向b | D. | Fe电极发生的反应为:Cu2++2e-=Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | 甲基橙溶液呈黄色的溶液,一定能大量存在的离子 | Na+、Fe3+、Cl-、SO42- |
| B | 在久置的氯水中能大量共存的微粒 | K+、Al3+、NO3-、HCOOH |
| C | 向明矾溶液中滴加Ba(OH)2溶液,恰好使Al3+沉淀完全: | 2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| D | 1L0.1mol/LCuSO4溶液和足量的Ca充分反应 | 最终生成6.4gCu |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com