
【题目】在373K时,把0.1mol![]() 气体通入体积为lL的恒容密闭容器中,立即出现红棕色。在60s时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法错误的是
气体通入体积为lL的恒容密闭容器中,立即出现红棕色。在60s时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法错误的是
A. 压缩容器,颜色加深
B. 在平衡时体系内含![]() 0.04mol
0.04mol
C. 以![]() 的浓度变化表示的平均反应速率为0.001mol/(L·s)
的浓度变化表示的平均反应速率为0.001mol/(L·s)
D. 平衡时,如果再充入一定量![]() ,则可提高
,则可提高![]() 的转化率
的转化率
【答案】D
【解析】
N2O4![]() 2NO2
2NO2
起始时物质的量(mol) 0.1 0
变化的物质的量(mol) x 2x
平衡时物质的量(mol) 0.1-x 2x
在恒温恒容条件下,气体的压强与气体的总物质的量成正比,在60s时,体系已达平衡,此时容器内压强为开始时的1.6倍,则:![]() =1.6,解得:x=0.06;
=1.6,解得:x=0.06;
A.压缩容器,反应物和生成物浓度增增大,此时平衡逆向移动,但根据勒夏特列原理,此时容器内气体颜色比原平衡深,故A正确;
B.由分析知,平衡时体系内含![]() 0.04mol,故B正确;
0.04mol,故B正确;
C.以![]() 的浓度变化表示的平均反应速率为
的浓度变化表示的平均反应速率为 =0.001mol/(L·s),故C正确;
=0.001mol/(L·s),故C正确;
D.由N2O4![]() 2NO2,平衡时如果再充入一定量N2O4,相当于增大压强,化学平衡逆向移动,N2O4的转化率降低,故D错误;
2NO2,平衡时如果再充入一定量N2O4,相当于增大压强,化学平衡逆向移动,N2O4的转化率降低,故D错误;
故答案为D。


科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. ![]() 在核磁共振氢谱中有5个吸收峰
在核磁共振氢谱中有5个吸收峰
B. 红外光谱图只能确定有机物中所含官能团的种类和数目
C. 质谱法不能用于相对分子质量的测定
D. 核磁共振氢谱、红外光谱和质谱都可用于分析有机物结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、铁、铝是重要的金属材料,铜、铁、铝及其化合物有非常重要的用途。
(1)高铁酸钾(K2FeO4)是一种高效多功能水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO 、OH 、FeO42、Cl 、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:________________________________。
②若反应过程中转移了 0.3mol 电子,则还原产物的物质的量为_______mol。
(2)以铝土矿(主要成分为Al2O3和Fe2O3、SiO2)为原料制备铝的一种工艺流程如下:
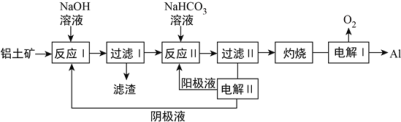
①滤渣主要成分为________。
②在实验室灼烧操作应选择的实验仪器为_________。
③反应II中,加入NaHCO3一段时间才有沉淀生成,写出加入少量NaHCO3时发生反应的离子方程式____________________________________。
(3)已知25 ℃时Ksp[Cu(OH)2]=2.2×1020,Ksp[Al(OH)3]=1.1×1033。在25 ℃下,向浓度均为0.1 mol·L1的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成_________沉淀(填化学式)。
(4)以含有少量硫酸的硫酸铜溶液为原料制备铜:a g铁粉与上述溶液完全反应后,得到a g铜,则参与反应的CuSO4与H2SO4的物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲配制3.6 mol/L的H2SO4溶液80 mL,探究硫酸的性质。实验室有两种不同浓度的硫酸可供选用:① 25%的硫酸(ρ=1.18 g/mL);②98%的硫酸 (ρ=1.8 g/mL)。请回答下列问题:
(1)配制该硫酸溶液应选用的玻璃仪器除量筒、烧杯和玻璃棒外还有________;
(2)本实验需量取所选用硫酸的体积为____________________mL;
(3)下列操作会使得所配硫酸溶液浓度偏低的是____________
a.量取硫酸溶液的量筒未用蒸馏水洗涤
b.硫酸稀释后立即转移至容量瓶中
c.转移的时候不小心有少许洒到实验台上
d.定容摇匀时,液面下降又加水
e.定容时仰视刻度线
(4)取所配硫酸溶液,往其中加入BaCl2溶液,观察有白色沉淀出现。试回答:如何证明溶液中的硫酸根离子沉淀完全?__________________________________;
(5)将100mL标号为②的浓硫酸与水(密度为1g/ml)混合,其质量分数为49﹪,则水的体
积________100mL(填“大于”、“小于”、“等于”或“无法确定”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
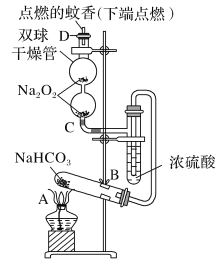
(1)在A试管内发生反应的化学方程式是_____。
(2)B装置的作用是_____。
(3)在双球干燥管内发生反应的化学方程式为____。
(4)双球干燥管内及D处观察到的实验现象是_____。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内及D处观察到的实验现象是:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积固定为a L的密闭容器中充入1 mol X气体和2 mol Y气体,发生反应X(g)+2Y(g)![]() 2Z(g),此反应达到平衡状态的标志是
2Z(g),此反应达到平衡状态的标志是
A. 容器内气体密度不随时间变化
B. 容器内气体的平均相对分子质量不随时间变化
C. 容器内X、Y、Z的浓度之比为1∶2∶2
D. 消耗0.1 mol X的同时生成0.2 mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KNO3和Ba(NO3)2两种固体混合物试回答下列问题
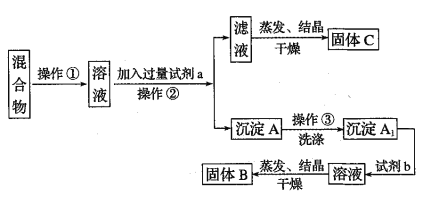
供选试剂:Na2SO4溶液、Na2CO3溶液、K2CO3溶液、K2SO4溶液、硫酸、硝酸
(1)试剂a是_______加入试剂b所发生反应的离子方程式为___________________________
(2)该方案能否达到实验目的:__________________________(填能或不能)若不能,应如何改进?__________________________(若能此问不用回答)
(3)若要测定原混合物中Ba(NO3)2的质量分数,除了要准确称量混合物的质量外至少还要获得的数据是__________的质量
(4)用所制备的KNO3固体配制0.1 mol/L KNO3溶液450mL,回答下列问题:
①配制过程中需要用到的玻璃仪器有烧杯、量筒、胶头滴管、______________
②需要用托盘天平称量_______g KNO3固体)
③下列情况会使所配溶液浓度偏低的是________
A.称量固体时,砝码与药品的位置放反了,即“左码右物”
B.使用有少量蒸馏水的容量瓶
C.定容时俯视刻度线观察液面
D.洗涤和转移时有液体外溅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. SO2![]() CaSO3
CaSO3![]() CaSO4
CaSO4
B. Fe![]() Fe2O3
Fe2O3![]() FeCl3
FeCl3
C. HCl(aq)![]() Cl2
Cl2![]() Ca(ClO)2
Ca(ClO)2
D. Cu2(OH)2CO3![]() CuO
CuO![]() CuCl2(aq)
CuCl2(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL0.1mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中逐滴滴入0.1mol·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是

A. a点时溶液中所含主要溶质为(NH4)2SO4
B. a→b段发生反应的离子方程式是 SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C. b点为最大沉淀量,对应的纵坐标值为0.02
D. c点加入Ba(OH)2溶液的体积为200 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com