
����Ŀ��������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Wԭ�ӵ�����������������������������
��ش��������⣺
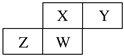
��1��Zλ�����ڱ��е�λ��______________��
��2��X��YԪ�ص��⻯���У����ȶ��Ե���________���ѧʽ����
��3��X����̬�⻯����������������Ӧ��ˮ���ﷴӦ���ɵĻ������д��ڵĻ�ѧ������Ϊ_________��
��4����д��X������������Ӧˮ�����ϡ��Һ���������۷�Ӧ�����ӷ�Ӧ����ʽ��______________��
���𰸡� �������ڵڢ�A�� H2O ���Ӽ������ۼ� Fe+4H++NO3-��Fe3++NO��+2H2O
��������������������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Wԭ�ӵ�����������������������������Wλ�ڵ������ڣ���W��P������X��N��Y��O��Z��Si�����Ԫ�������ɽ����
������������Ϸ�����֪X��N��Y��O��Z��Si��W��P����
��1��Z��Si��λ�����ڱ��е�λ��Ϊ�������ڵڢ�A�塣
��2���ǽ�����Խǿ���⻯��Խ�ȶ����ǽ�������O��N����X��YԪ�ص��⻯���У����ȶ��Ե���H2O��
��3��X����̬�⻯�ﰱ����������������Ӧ��ˮ�������ᷴӦ���ɵĻ�����������泥����д��ڵĻ�ѧ������Ϊ���Ӽ������ۼ���
��4��X������������Ӧˮ�����ϡ��Һ��ϡ���ᣬ���������۷�Ӧ�����ӷ�Ӧ����ʽΪFe+4H++NO3-��Fe3++NO��+2H2O��


 ����ѧ����ϵ�д�
����ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������dzµ��㡱������Ϊ�����������������������ζ��������������ʵ��������Ҳ��������ͼ��ʾ��װ����ȡ�����������ش��������⡣

(1)��ϩ��ȡ�Ҵ��Ļ�ѧ����ʽ��__________________________��
(2)д����ȡ���������Ļ�ѧ��Ӧ����ʽ��________________________��
(3)Ũ��������ã�_______________________________��
(4)����̼������Һ����Ҫ������________________________________________��
(5)װ���е���Ҫ�ڱ���̼������Һ��Һ���ϣ����ܲ�����Һ�У�Ŀ����__________��
(6)��Ҫ���Ƶõ������������������Ӧ�ò��õ�ʵ�������___________________��
(7)����ʵ��ʱ����ʱ��Ҫ��ʢ�������������Թ�����뼸�����Ƭ����Ŀ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽ��������������Na2SO4��ˮ��ԭ����ͼ��ʾ�����ö��Ե缫��ab��cd��Ϊ���ӽ���Ĥ����ֱ���糡�������£���Ĥ�м��Na+��SO42-��ͨ�����ӽ���Ĥ�������˸��������ӱ��赲���ܽ����м���ҡ�����������ȷ����

A. ͨ����м���ҵ�SO42-����������Ǩ�ƣ���������ҺpH����
B. �÷��ڴ�����Na2SO4��ˮʱ���Եõ�NaOH��H2SO4��Ʒ
C. ������ӦΪ2H2O�C4e�C=O2+4H+����������ҺpH����
D. ����·��ͨ��1mol���ӵĵ���ʱ������0.5mol��O2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������е����⣬�뽺�������ص��ǣ� ��
A.�����еľ������װ��B.Ϳ�ϡ�īˮ������
C.������Ⱦ�ij�����D.����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X�pY�pZ�pW�pQ��ԭ������������Xԭ�Ӻ��������������Ǵ�����������2����Y�ķ�����YF3�����и�ԭ�Ӿ����������8�����ȶ��ṹ��Z�pW�dz���������Z��ͬ������ԭ�Ӱ뾶����Ԫ�ء�W�ļ�������ͬ���������Ӱ뾶��С�ġ�X��Zԭ������֮����Q��ԭ��������ȡ�����˵����ȷ����
A. ��ͬ������Z��W���ʷֱ�������ϡ���ᷴӦʱ��Z�ĵ��ʻ�õ�������
B. X��Q�γɵĻ������Z��Q�γɵĻ�����Ļ�ѧ��������ͬ
C. ����������Ӧ��ˮ��������ԣ�X��W
D. Y�ļ���̬�⻯����Q�ĵ��ʷ�Ӧ�������Dz�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ�����Ʊ�Cl2��ͨ��FeCl2��Һ�л��FeCl3��Һ�IJ���װ�á�
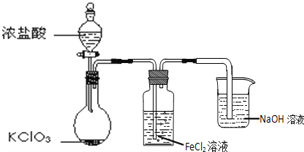
��1��NaOH��Һ��������______��
��2��ʵ���У�����������������ٶȣ��Ա�ʹFeCl2��Һת����ȫ���������������ٶȵIJ�����______��
��3����ʼ��Ӧ����ϴ��ƿ���ձ���ʢ�ŵ������У�����������______���ѧʽ����
��4����ƿ�з�����Ӧ�Ļ�ѧ����ʽ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ������ͬ��Ԫ��֮�����(����)
A. Zn+2HCl![]() ZnCl2+H2��
ZnCl2+H2��
B. 2H2S+SO2![]() 3S��+2H2O
3S��+2H2O
C. H2+CuO![]() Cu+H2O
Cu+H2O
D. 2H2O![]() 2H2��+O2��
2H2��+O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ѧ�о���ѧϰС�������ʵ����֤Zn��Fe��Cu�Ľ�����ԣ�����������������ַ��������������������й�ʵ����Ŀ��
��1�������ֽ��������ᷴӦ���������жϣ�ʵ���г�ѡ���С��ͬ�Ľ���Ƭ�⣬����Ҫ����________��________��ͬ����ѡ��һ������Һ��֤���ֽ����Ļ����ԣ����Լ�________��
��2��������Zn��Cu���缫��Ƴ�ԭ��أ����ܲ��������ȶ��ĵ�������ȷ��Zn��Cu�Ļ�ԣ��������淽���л���ԭ���װ��ͼ�����ԭ��صĵ缫���Ϻ͵������Һ_______��

������װ����������ӦʽΪ��________��
��ijС��ͬѧ����Zn��Fe��Ϊ�缫��ֻ��һ��ԭ���֤�����ֽ����Ļ�ԣ���������Һ���ѡ��________��
A.0.5molL��1�Ȼ�������Һ
B.0.5molL��1�Ȼ�ͭ��Һ
C.0.5molL��1����
D.0.5molL��1�Ȼ�������0.5molL��1�Ȼ�ͭ�����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��������̼���⡢������Ԫ����ɣ���������ͼֻ��C��H����O��H����C��O���������գ����л������Է���������60������л���Ľṹ��ʽ��
A. CH3CH2OCH3 B. CH3CH(OH)CH3 C. CH3CH2CH2CH2OH D. CH3COOH
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com