
| A | B | C | D | |
| 环境污染 |  白色污染 |  雾霾 |  臭氧空洞 |  酸雨 |
| 产生原因 | 聚乙烯等塑料 | 胶体的丁达尔效应 | 氟利昂的泄漏 | 煤的直接燃烧 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.白色污染与塑料的使用有关;
B.雾霾与汽车尾气的排放有关;
C.臭氧空洞与含氟化合物的使用有关;
D.酸雨与二氧化硫的排放有关.
解答 解:A.塑料的大量使用,且难以降解,则造成白色污染,故A正确;
B.汽车尾气的排放,使空气中PM2.5含量增加,导致雾霾发生,但雾霾不一定为胶体,如云、雾等属于胶体,但不是雾霾,故B错误;
C.含氟化合物的排放,使臭氧层破坏,导致臭氧空洞,故C正确;
D.煤的直接燃烧,二氧化硫的排放使雨水的酸性增强,形成酸雨,故D正确;
故选B.
点评 本题考查环境污染问题,为高频考点,侧重于化学与生活、环境的考查,有利于培养学生良好的科学素养,把握常见的环境污染问题及环境污染物、形成原因为解答的关键,注重化学与生活的联系,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 同系物不一定符合同一通式 | |
| B. | 同分异构体不一定具有相同的最简式 | |
| C. | 相对分子质量相等的两种有机物必定是同分异构体 | |
| D. | 同分异构体间不一定有相似的化学性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C |
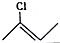 |  |  |
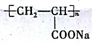 .
.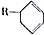 结构,D可能的结构有4种;写出
结构,D可能的结构有4种;写出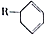 和Cl2发生1,4-加成反应的化学方程式:
和Cl2发生1,4-加成反应的化学方程式: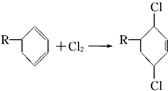 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
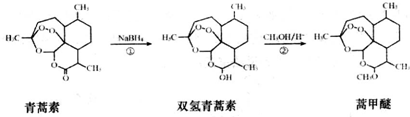
| A. | 青蒿素的分子式是C15H22O5,属于烃的衍生物 | |
| B. | 青蒿素难溶于水,而易溶于有机溶剂 | |
| C. | 反应②为取代反应,有H2O生成 | |
| D. | 青蒿素遇湿润的淀粉碘化钾试纸立刻显蓝色,是因为分子结构中含有酯基 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A.B,C,D,E五种元素,均位于元素周期表的前四周期.它们的核电荷数逐渐增加.且核电荷数之和为57;B原子的L层p轨道中有2个电子,C的原子核外有三个未成对电子,D与B原子的价电子数相同.E原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.请回答下列问题:
A.B,C,D,E五种元素,均位于元素周期表的前四周期.它们的核电荷数逐渐增加.且核电荷数之和为57;B原子的L层p轨道中有2个电子,C的原子核外有三个未成对电子,D与B原子的价电子数相同.E原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.请回答下列问题: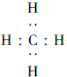 ,Y中D原子的杂化轨道类型为sp3杂化;C与A形成的常见化合物的分子构型为三角锥形.
,Y中D原子的杂化轨道类型为sp3杂化;C与A形成的常见化合物的分子构型为三角锥形.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若容积为某一固定值,当体系的压强不再发生变化时说明达到化学平衡状态 | |
| B. | 若上述可逆反应达化学平衡状态后,给平衡体系加压(缩小容积,其他条件不变),则容器内气体的平均摩尔质量将减小 | |
| C. | 若上述可逆反应达到化学平衡状态后,升高温度(其他条件不变)体系颜色加深,则Q>0 | |
| D. | 对于上述可逆过程给平衡体系减压(增大容积,其他条件不变),可以提高N2O4的产率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在 pH 为 6.37 及 10.25 时,溶液中 c(H2CO3)=c(HCO3-)=c(CO32-) | |
| B. | 反应 HCO3-+H2O?H2CO3+OH-的平衡常数为 10-7.63 | |
| C. | 0.1 mol•L-1NaHC2O4溶液中 c(HC2O4-)+2c(C2O42-)+c(H2C2O4)=0.1 mol•L-1 | |
| D. | 往 Na2CO3溶液中加入少量草酸溶液,发生反应:CO32-+H2C2O4=HCO3-+HC2O4- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
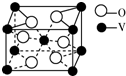 钒及其化合物非常丰富.钒可用于生产合金钢、航天用的钒钛合金及化工催化剂等.
钒及其化合物非常丰富.钒可用于生产合金钢、航天用的钒钛合金及化工催化剂等.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com