
高温下,某反应达平衡,平衡常数K= 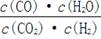 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
| A.反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为CO + H2O  CO2+ H2 CO2+ H2 |
A
解析试题分析:化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,据此可知该反应的化学方程式是CO2+ H2 CO + H2O,D不正确;反应前后气体的体积是不变,则增大压强,平衡不移动,但氢气的浓度增加,B不正确;恒容时,温度升高,H2浓度减小,这说明升高温度平衡向正反应方向移动,所以正反应是放热反应,A正确;升高温度,正逆反应速率都是增大,C不正确,答案选A。
CO + H2O,D不正确;反应前后气体的体积是不变,则增大压强,平衡不移动,但氢气的浓度增加,B不正确;恒容时,温度升高,H2浓度减小,这说明升高温度平衡向正反应方向移动,所以正反应是放热反应,A正确;升高温度,正逆反应速率都是增大,C不正确,答案选A。
考点:考查平衡常数的应用和外界条件对平衡状态的影响
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,难易适中。在注重对学生基础知识考查与训练的同时,侧重对学生灵活运用基础知识解决实际问题的能力的培养,有利于培养学生的逻辑推理能力,提升学生的学科素养。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| A、该反应的焓变为负值 | |||
B、该反应化学方程式为CO+H2O
| |||
| C、恒温恒容下,充入CO2,H2浓度一定减小 | |||
| D、升高温度,逆反应速率减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com