
(1)已知在常温常压下:
① 2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol-1
② H2O(l) H2O(g) △H= + 44.0 kJ.mol-1
写出表示甲醇燃烧热的热化学方程式 。
(2)甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
| 方法一 | CO(g) +2H2(g) |
| 方法二 | CO2(g) +3H2(g) |
工业上可用如下方法合成甲醇:
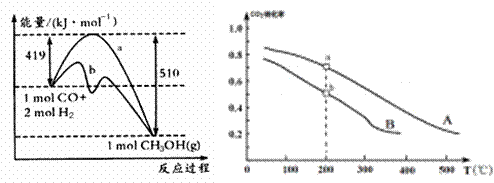
方法一 方法二
①方法一:该反应的△S 0(填“>”或“<”)。图中曲线a到曲线b的措施是
,恒温恒容时,下列说法能说明反应到达平衡状态的是 。
A.体系的平均摩尔质量不再改变 B. V(CO)= V(CH3OH)
C. H2的转化率达到了最大限度 D. △H不再改变
②方法二:将CO2和H2按物质的量之比1:3充入体积为2.0L的恒容密闭容器中反应,如图两条曲线分别表示压强为0.1 MPa和5.0 MPa下CO2转化率随温度的变化关系,其中a点的平衡常数表达式为: ;a,b两点化学反应速率别用Va、Vb表示,则Va Vb(填“大于”、“小于”或“等于”)。 已知原子利用率=期望产物的总质量与生成物的总质量之比,则方法一的原子利用率是方法二的原子利用率的
倍(保留两位小数).
甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是通电后将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。写出除去甲醇的离子方程式 。
【知识点】燃烧热、盖斯定律、化学平衡的综合应用
【答案解析】(1)CH3OH(l)十 O2(g) CO2(g)+2H2O(l) △H= -725.8kJ·mol-1 (2分)
O2(g) CO2(g)+2H2O(l) △H= -725.8kJ·mol-1 (2分)
(2)①<(1分) 加入催化剂 (2分) AC(2分)
② (2分) 大于(2分)1.56 (2分)
(2分) 大于(2分)1.56 (2分)
(3) 6Co3++CH3OH+H2O=CO2↑+6Co2++6H+(2分)
解析:(1)燃烧热是指1mol可燃物完全燃烧生成稳定化合物所放出的热量,书写热化学方程式时,注意可燃物前面的计量数为1;运用盖斯定律,①/2-2×②得:
CH3OH(l)十 O2(g) CO2(g)+2H2O(l) △H= -725.8kJ·mol-1
O2(g) CO2(g)+2H2O(l) △H= -725.8kJ·mol-1
方法一:CO(g) +2H2(g) 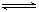 CH3OH(g),这是个熵减的反应,△S<0;图中曲线a到曲线b的变化是降低了反应所需的最高能量,改变的条件是催化剂;恒温、恒容时:A、反应是非等体反应,体系的平均摩尔质量不改变,可以作为平衡的判据,故A正确;B、不能表明正逆反应速率相等,故B错误;C、H2的转化率达到了最大限度,说明平衡不再移动,故C正确;D、反应热只与温度有关,故D错误。
CH3OH(g),这是个熵减的反应,△S<0;图中曲线a到曲线b的变化是降低了反应所需的最高能量,改变的条件是催化剂;恒温、恒容时:A、反应是非等体反应,体系的平均摩尔质量不改变,可以作为平衡的判据,故A正确;B、不能表明正逆反应速率相等,故B错误;C、H2的转化率达到了最大限度,说明平衡不再移动,故C正确;D、反应热只与温度有关,故D错误。
②方法二:CO2(g) +3H2(g) 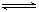 CH3OH(g) +H2O(g),平衡常数表达式为
CH3OH(g) +H2O(g),平衡常数表达式为 ;增大压强,平衡正向移动,CO2的转化率增大,则A表示的压强大,等温条件下,压强越大,反应速率加快,故Va大于Vb;原子利用率=期望产物的总质量与生成物的总质量之比,方法一的原子利用率=100%,方法二的原子利用率=32/(32+18)=64%,
;增大压强,平衡正向移动,CO2的转化率增大,则A表示的压强大,等温条件下,压强越大,反应速率加快,故Va大于Vb;原子利用率=期望产物的总质量与生成物的总质量之比,方法一的原子利用率=100%,方法二的原子利用率=32/(32+18)=64%,
则方法一的原子利用率是方法二的原子利用率的100/64=1.56
(3)要消除甲醇的污染,Co3+做氧化剂把甲醇氧化成CO2,氧化还原反应:
6Co3++CH3OH+H2O=CO2↑+6Co2++6H+
【思路点拨】本题主要考察燃烧热的热化学方程式的书写,有关化学平衡的综合应用是高考的重点,学会分析图像,用“定一议二”的方法。平衡判断问题需要细心,注意方法的归纳及反应的特点。难度不是太大。


科目:高中化学 来源: 题型:
标准状况下将 aL HCl气体溶于bmL水中,得到的盐酸溶液密度为c g·cm-3,则该溶液中溶质的物质的量的浓度可表示为( )
A.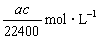 B.
B.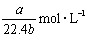
C.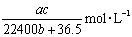

 D.
D.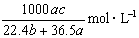
查看答案和解析>>
科目:高中化学 来源: 题型:
2004年2月22日是第35个 “世界地球日”,我国确定的主题是“善待地球——科学发展”。下列行为中不符合这一主题的是( )
A.采用“绿色化学”工艺,使原料尽可能转化为所需要的物质
B.减少直至不使用对大气臭氧层起破坏作用的氟氯烃
C.大量开采地下水,以满足社会对水的需求
D.节约能源,提高能源利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D四种物质具有以下物理性质:
| A | B | C | D | |
| 分散到水中 | 得悬浊液 | 得无色溶液 | 液体分层,且下层为无色油状液体 | 得无色溶液 |
| 熔点(℃) | 1452 | -21.3 | -11.5 | 801 |
| 沸点(℃) | 1703 | 78.9 | 117 | 1210 |
(1)已知A与D不发生反应,且均不与水反应。
①.欲从A、D的混合物中分离提纯D,需进行的操作是:
a:溶解;b: (填操作名称,下同);c: 。
②上述a、b、c操作过程中均需用到的一种玻璃仪器为_____;从B的水溶液中分离出B的操作名称为 。
(3)从C与水的混合物中分离提纯C所需的玻璃仪器有_______
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表有许多有趣的编排方式,有同学将短周期元素按照原子序数递增的顺序进行排列得到如图所示的“蜗牛”元素周期表。图中每个“·”代表一种元素(图中字母不表示元素符号)。下列说法正确的是
A.L、M、X三元素位于同一族
B.K、Z两元素的氢化物的水溶液都显酸性
C.Y元素对应的氢化物比K元素对应的氢化物沸点低
D.K、L、X、Z四种元素离子半径大小顺序是Z->L+>X3+>K3-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的分子中既有σ键,又有π键的是
①HCl ②H2O ③N2 ④H2O2 ⑤C2H4 ⑥C2H2
①②③ B.③④⑤⑥ C.①③⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转
B.分子中键能越大,键长越长,则分子越稳定
C.含有π键的化合物与只含σ键的化合物的化 学性质不同
学性质不同
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.在[Cu(NH3)4] 2+离子中,Cu2+给出孤对电子,NH3提供空轨道
C.向反应后的溶液加入乙醇,溶液没有发生变化
D.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4] 2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com