
【题目】已知1mol白磷变成1mol红磷放出18.39kJ的热量。下列两个方程式:
4P(白磷,s)+ 5O2(g)= 2P2O5(s);△H1
4P(红磷,s)+ 5O2(g)= 2P2O5(s);△H2
则△H1和△H2的关系正确的是
A.△H1 = △H2 B.△H1 > △H2 C.△H1 < △H2 D.不能确定
科目:高中化学 来源: 题型:
【题目】5.4g水与_ ___g硫酸所含的分子数相等,它们所含氧原子数之比是_ ___ ,其中氢原子数之比是_ ___ 。若将上述硫酸配成500mL溶液,所得溶液的溶质的物质的量浓度为_ ___ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料—光导纤维,C与烧碱反应生成含A元素的化合物D
(1)B元素的原子最外层电子数与A相同,则B在元素周期中的位置___ __.
(2)写出易与C发生反应的酸与C反应的化学方程式是______________.
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E:将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F.
①写出生成D的化学反应方程式:______________.
②要将纯碱高温熔化,下列坩埚中不可选用的是__________.
A.普通玻璃坩埚 | B.石英玻璃坩埚 | C.铁坩埚 | D.瓷坩埚. |
③将过量的E通入D的溶液中发生反应的离子方程式是:_________________。
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏伽德罗常数,下列说法中正确的是
A.标况下,22.4L 的H2O 含有的水分子数为NA
B.标况下,11.2LCCl4 中含有的Cl 原子数为2NA.
C. 17gNH3中含有的电子总数为l0NA
D. 0.5mol/L的H2SO4溶液中含有的H+数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对进行焰色反应实验操作注意事项的说明正确的是 ①要透过蓝色的钴玻璃观察钾的火焰颜色 ②先把铂丝烧到与原来火焰颜色相同,再蘸取被检测的物质 ③每次实验后,要用盐酸把铂丝洗净 ④实验时最好选择本身较微弱的火焰 ⑤没有铂丝,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确C.仅有⑤不正确 D.全对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下图所示装置来试验用粗铁粒与某浓度稀硝酸反应制取NO气体。
(1)当打开开关a,关闭开关b时,A中干燥管中观察到的实验现象是 ,烧杯B中盛的是 溶液。当 时关闭开关a,打开开关b,此时C中用排水法收集NO气体。当C中收满气体后,关闭开关b,装置A中观察到的现象是① ;② 。
(2)将a mol Fe与含b mol HNO3的稀溶液充分反应后,若硝酸的还原产物只有NO。试讨论分析烧杯A中最后溶液的主要阳离子组成及其物质的量,将结果填入下表未完成的空格中。
a/b取值范围 | 最终溶液中的主要阳离子及其物质的量 |
<1/4 | |
=1/4 | a mol Fe3+ |
大于1/4小于3/8 | |
=3/8 | a mol Fe2+ |
>3/8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料。
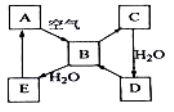
(1)写出A在加热条件下与H2反应的化学方程式________________
(2)写出E与A的氢化物反应生成A的化学方程式___________________________
(3)写出一个由D生成B的化学方程式___________________________;
(4)将5mL0.10mol·L-1的E溶液与10mL0.10 mol·L-1的NaOH溶液混合。写出反应的离子方程式________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)若某药品质量约为32.0g, 托盘天平准确称其质量,若用↓表示在右盘放上砝码,用↑表示将砝码取下,在下列表格的空格内,用↓和↑表示相应砝码的放上或取下.
50g | 20g | 20g | 10g | 5g |
(2)配制500mL 0.1mol.L-1 Na2CO3溶液,图中操作②中应该填写的数据为__________,实验操作的先后顺序为________________ (填编号)。
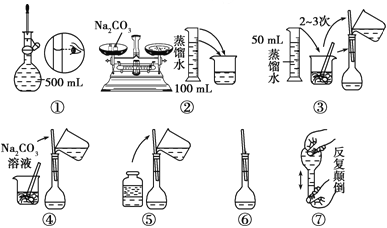
(3)在配制一定物质的量浓度的溶液时,用“偏高、偏低、无影响”表示下列操作对所配溶液浓度的影响。
①用量筒取液态溶质,读数时,俯视量筒,所配制溶液的浓度___________
②将量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶,所配制溶液的浓度___________
③定容摇匀后,有少量溶液外流,对所配制溶液的浓度___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com