
| A. | Cl2是氧化剂,KOH是还原剂 | |
| B. | KOH是氧化剂,Cl2是还原剂 | |
| C. | KCl是还原产物,KClO3是氧化产物 | |
| D. | 被氧化的氯原子与被还原的氯原子数之比为5:1 |
分析 A、化合价升高元素所处的反应物为还原剂,化合价降低元素所在的反应物为氧化剂;
B、氢氧化钠中各元素的化合价不变,氯气中的氯元素的化合价既升高又降低;
C、化合价升高元素所处的生成物为氧化产物,化合价降低元素所在的生成物为还原产物;
D、根据反应确定氧化剂和还原剂,进而确定它们的量关系.
解答 解:A、化合价变化的元素只有氯元素,氯气既是氧化剂又是还原剂,故A错误;
B、氢氧化钠中各元素的化合价不变,所以氢氧化钠既不是氧化剂也不是还原剂,氯气中的氯元素的化合价既升高又降低,则氯气既是氧化剂又是还原剂,故B错误;
C、KClO3为氧化产物,KCl为还原产物,故C正确;
D、6mol氯原子中,做氧化剂的占5mol,做还原剂的占1mol,所以氧化剂质量是还原剂质量的5倍,被氧化的氯原子与被还原的氯原子数之比为1:5,故D错误.
故选C.
点评 本题考查氧化还原反应的特征和有关的概念内涵,要求学生具有分析和解决问题的能力,注意反应中只有一种元素化合价变化时的情况,难度较大.


科目:高中化学 来源: 题型:选择题
| A. | NO分解反应NO(g)?$\frac{1}{2}$N2(g)+$\frac{1}{2}$O2(g)的平衡常数为1×10-30 | |
| B. | 根据K2的值可以判断常温下H2和O2很容易反应生成H2O | |
| C. | 常温下,NO、H2O、CO2三种物质分解放出O2的倾向顺序为NO>H2O>CO2 | |
| D. | 温度升高,上述三个反应的平衡常数均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入硝酸酸化,再滴加KSCN溶液后有红色物质生成,则原溶液中一定有Fe3+存在 | |
| B. | 加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO32-存在 | |
| C. | 某溶液做焰色反应时火焰为黄色,则该溶液中一定有钠元素 | |
| D. | 分别含有Mg2+、Cu2+、Fe2+和Na+的四种盐溶液,只用NaOH溶液不能一次性鉴别开 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
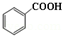 +C2H5OH$\stackrel{H_{2}SO_{4}}{?}$
+C2H5OH$\stackrel{H_{2}SO_{4}}{?}$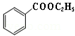 +H2O
+H2O| 沸点(℃) | 密度(g•cm-3) | |
| 苯甲酸 | 249 | 1.2659 |
| 苯甲酸乙酯 | 212.6 | 1.05 |
| 乙醇 | 78.5 | 0.7893 |
| 环已烷 | 80.8 | 0.7785 |
| 乙醚 | 34.51 | 0.7318 |
| 环已烷、乙醇和水共沸物 | 62.1 |
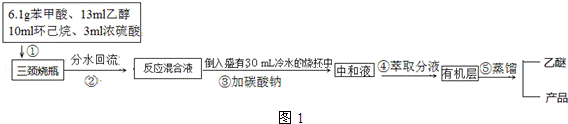
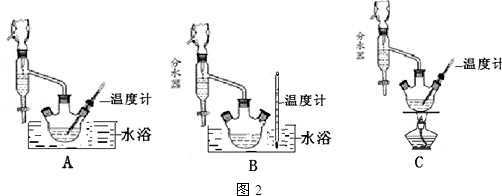
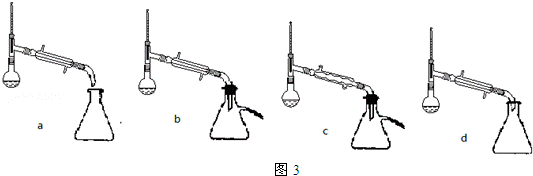
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
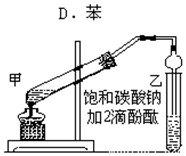 实验室制取乙酸乙酯的主要步骤如下:
实验室制取乙酸乙酯的主要步骤如下: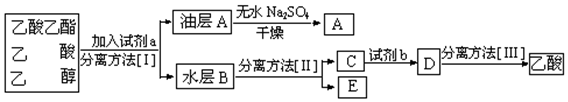
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化钠水解:S2-+2H2O?H2S↑+2OH- | |
| B. | 硫氢化钠水解:HS-+H2O?H3O++S2- | |
| C. | 硫化钾水解:S2-+H2O?HS-+OH- | |
| D. | 硫酸铝溶液跟碳酸氢钠溶液反应:Al3++3HCO3-+6H2O?Al(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 产物不稳定,受热即脱水而生成不饱和醛.
产物不稳定,受热即脱水而生成不饱和醛.
 ;F
;F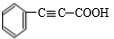 .
. +CH3CHO$\stackrel{△}{→}$
+CH3CHO$\stackrel{△}{→}$ +H2OE→F
+H2OE→F +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$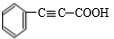 +2NaBr+2H2O
+2NaBr+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有AgCl 沉淀 | B. | 只有AgI 沉淀 | ||
| C. | AgCl、AgI 都沉淀,以AgCl 为主 | D. | AgCl、AgI 都沉淀,以AgI 为主 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com