
����Ŀ��A����Ȼ������Ҫ�ɷ֣���AΪԭ����һ�������¿ɻ���л���B��C��D��E��F�����ת����ϵ��ͼ����֪��B�ڱ�״���µ��ܶ�Ϊ1.06g��L-1��C�ܷ���������Ӧ��FΪ��Ũ����ζ����������ˮ����״Һ�塣

��ش�
(1)�л���D�к��еĹ�����������__________________��
(2) D+E��F�ķ�Ӧ������_________________________��
(3)�л���A�ڸ�����ת��ΪB�Ļ�ѧ����ʽ��_________________��
(4)����˵����ȷ����___��
A.�л���E������Ʒ�Ӧ��ˮ������Ʒ�ӦҪ����
B.�л���D��E��F���ñ���Na2CO3��Һ����
C.ʵ�����Ʊ�Fʱ��Ũ������Ҫ����������
D.�л���C�ܱ����Ƽ���������ͭ����Һ������KMnO4��Һ����
���𰸡� �Ȼ� ������Ӧ 2CH4![]() C2H2+3H2 BD
C2H2+3H2 BD
��������A����Ȼ������Ҫ�ɷ֣�A�Ǽ��顣��AΪԭ����һ�������¿ɻ���л���B��C��D��E��F����֪��B�ڱ�״���µ��ܶ�Ϊ1.16g��L-1��B����Է���������1.16��22.4��26������B����Ȳ��C�ܷ���������Ӧ��˵����Ȳ��ˮ�ӳ�������ȩ����ȩ�����������ᣬE�����ᡣ��ȩ����ԭ�����Ҵ���D���Ҵ����Ҵ���������������FΪ��Ũ����ζ��������������������ˮ����״Һ�塣(1)�л���D���Ҵ������к��еĹ������������ǻ���(2) D+E��F�ķ�Ӧ������������Ӧ��(3)�л���A�ڸ�����ת��ΪB������ԭ���غ��֪�����������ɣ���Ӧ�Ļ�ѧ����ʽ��2CH4![]() C2H2+3H2��(4)A.�Ҵ����ǵ���ʣ��л���D������Ʒ�Ӧ��ˮ������Ʒ�ӦҪ����A����B.�Ҵ���ˮ���ܣ������̼���Ʒ�Ӧ����CO2����������������ˮ���Ҵ��л���D��E��F���ñ���Na2CO3��Һ����B��ȷ��C.ʵ�����Ʊ�Fʱ��Ũ������Ҫ���������ˮ�����ã�C����D.�л���C����ȩ���ܱ����Ƽ���������ͭ����Һ������KMnO4��Һ������D��ȷ����ѡBD��
C2H2+3H2��(4)A.�Ҵ����ǵ���ʣ��л���D������Ʒ�Ӧ��ˮ������Ʒ�ӦҪ����A����B.�Ҵ���ˮ���ܣ������̼���Ʒ�Ӧ����CO2����������������ˮ���Ҵ��л���D��E��F���ñ���Na2CO3��Һ����B��ȷ��C.ʵ�����Ʊ�Fʱ��Ũ������Ҫ���������ˮ�����ã�C����D.�л���C����ȩ���ܱ����Ƽ���������ͭ����Һ������KMnO4��Һ������D��ȷ����ѡBD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A��1 mol CH4ȼ�շų�����������ȼ����
B��1 mol Cȼ������COʱ�ų�����������C��ȼ����
C��1 mol H2ȼ������ˮ�ų�����������H2��ȼ����
D����ͬ��������1 mol H2O(l)��ȫ�ֽ����յ�������H2��O2��������1 mol H2O(l)�ų�����������ֵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܺ����ᷴӦ�����ܺ�����������Һ��Ӧ�������ǣ� ��
A.Fe
B.Fe2O3
C.Al
D.AlCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����m��Al2O3��Fe2O3�Ļ�����ܽ��ڹ�����100mLpHֵΪ1��������,Ȼ�������м���NaOH��ҺʹFe3+��Al3+�պ�ȫ��ת���ɳ���,��ȥNaOH��Һ100mL,��NaOH��Һ��Ũ��Ϊ
A. 0.1mol/L B. 0.05mol/L C. 0.2mol/L D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeSO4���ȷֽ�Ļ�ѧ����ʽΪ��2FeSO4![]() Fe2O3+SO2��+SO3��
Fe2O3+SO2��+SO3��
��ش�
��FeSO4���Ȳ��������尴ͼʾװ�ý���ʵ�飬֤ʵ����SO2��SO3����˵��SO2���ڵ�ʵ��������_______��Ϊ�ⶨBaSO4�����������������IJ�����������Ϊ____��ϴ�ӡ����������
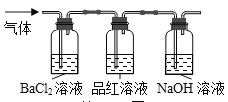
�Լ�һ��ʵ�鷽�����û�ѧ������֤FeSO4���Ⱥ����ijɷ�(������������Ӧ)_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��װ����ƺ�������ȷ����
A | B | C | D |
|
|
|
|
Һ��ֲ㣬 �²����ɫ | �жϷǽ����ԣ� Cl��C��Si | �ձ����ȳ��ְ�ɫ������������ܽ� | ̽���Ӵ�����Է�Ӧ���ʵ�Ӱ�� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽBa2++2OH+2H++SO4 2![]() BaSO4��+2H2O����ʾ�ķ�Ӧ��
BaSO4��+2H2O����ʾ�ķ�Ӧ��
A. ��������Һ�м����Ȼ�����Һ
B. ��������Һ�м�������������Һ
C. ���Ȼ������������ƵĻ����Һ�м�������������Һ
D. ������������Һ�����������������Ļ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ2 L��3���ܱ������з�����Ӧ3A(g)��B(g)![]() xC(g)������ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ�й��������£�
xC(g)������ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ�й��������£�
���� | �� | �� | �� |
��Ӧ��Ͷ���� | 3 mol A��2 mol B | 6 mol A��4 mol B | 2 mol C |
����ƽ���ʱ��/min | 5 | 8 | |
A��Ũ��/(mol��L��1) | c1 | c2 | |
C��������� | w1 | w3 | |
��������ܶ�/(g��L��1) | ��1 | ��2 |
����˵����ȷ���� (����)
A. ��x��4����2c1��c2 B. ��w3��w1���ɶ϶�x��4
C. ����x��ֵ�Ƕ��٣�����2��1����2 D. �������з�Ӧ�ӿ�ʼ����ƽ��ƽ������Ϊv(A)��0.3 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���Թ�ҵ��ˮ�к���K2Cr2O7 �������£�����(H2C2O4)�ܽ����е�Cr2O![]() ת��ΪCr3����ij������Ϊ��һ���о��й����ضԸ÷�Ӧ���ʵ�Ӱ�죬̽�����£�
ת��ΪCr3����ij������Ϊ��һ���о��й����ضԸ÷�Ӧ���ʵ�Ӱ�죬̽�����£�
��1����25 ���£����ƹ���ǿ�ȡ���ˮ��Ʒ��ʼŨ�Ⱥʹ���������ͬ�����ڲ�ͬ�ij�ʼpH��һ��Ũ�Ȳ�����Һ���������Ա�ʵ�飬�������ʵ����Ʊ���
ʵ���� | ��ʼpH | ��ˮ��Ʒ���/mL | ������Һ���/mL | ����ˮ���/mL |
�� | 4 | 60 | 10 | 30 |
�� | 5 | 60 | 10 | 30 |
�� | 5 | 60 | 20 | a=___________ |
���ʵ��ٺ͢���Һ�е�Cr2O![]() Ũ����ʱ��仯��ϵ��ͼ��ʾ��
Ũ����ʱ��仯��ϵ��ͼ��ʾ��
��2��������Ӧ����ᱻ����Ϊ____________________(�ѧʽ)��
��3��ʵ��ٺ͢ڵĽ������_______________________________��
��4��ʵ�����0��t1ʱ��η�Ӧ����v(Cr3��)��___________________mol��L��1��min��1(�ô���ʽ��ʾ)��

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com