
【题目】(1)分别用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
①Mg(Al)
试剂:________;离子方程式:_____________________。
②CO2(HCl)
试剂:________;离子方程式:_____________________。
(2)把下列离子方程式改写成化学方程式。
①2H++CO![]() CO2↑+H2O_____________________。
CO2↑+H2O_____________________。
②Al3++3OH—Al(OH)3↓_______________________。
【答案】 NaOH 2Al +2OH—+ 2H2O=2AlO2—+3H2↑ 饱和NaHCO3溶液 HCO![]() +H+===H2O+CO2↑ Na2CO3+H2SO4Na2SO4+CO2↑+H2O AlCl3+3NaOH == Al(OH)3↓
+H+===H2O+CO2↑ Na2CO3+H2SO4Na2SO4+CO2↑+H2O AlCl3+3NaOH == Al(OH)3↓
【解析】(1)本题考查物质的除杂,①Mg和Al都活泼金属,都能与酸反应,但Al能与氢氧化钠反应,Mg不与氢氧化钠反应,因此所加除杂试剂为NaOH溶液,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;②除杂时能把杂质转化成目标物质,利用盐酸的酸性比碳酸强,用盐酸得到CO2,但不能用Na2CO3溶液,因为CO2与Na2CO3反应生成NaHCO3,因此使用饱和的碳酸氢钠的溶液,HCO3-+H+=CO2↑+H2O;(2)本题考查离子反应方程式改写成化学反应方程式,①酸用强酸,碳酸盐是可溶的,不能伴随其他反应,因此酸可以用硝酸、盐酸、硫酸,碳酸盐可以是碳酸钠,也可以是碳酸钾,因此反应方程式为2HCl+Na2CO3=2NaCl+CO2↑++H2O,或者Na2CO3+H2SO4=Na2SO4+CO2↑+H2O;②用可溶性铝盐和强碱反应,因此AlCl3+3NaOH=Al(OH)3↓+3NaCl。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 核素14C的中子数是6
B. 35Cl和37Cl互为同位素
C. O2和O3互为同素异形体
D. CH3CH2O H和CH3OCH3互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1 mol X、3 mol Y充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g) +3Y(g) ![]() 2Z(g);ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是 ( )
2Z(g);ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是 ( )
A.升高温度,X的体积分数减小
B.缩小体积,Y的物质的量浓度不变
C.保持容器体积不变,充入1mol的稀有气体He,Z的浓度不变
D.保持容器体积不变,充入2mol的Z(g),X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、蒸馏、萃取
B.萃取、蒸馏、分液
C.分液、萃取、蒸馏
D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关混合物、纯净物、电解质、非电解质的正确组合为
纯净物 | 混合物 | 电解质 | 非电解质 | |
A. | 纯盐酸 | 水煤气 | 硫酸 | 干冰 |
B. | 蒸馏水 | 蔗糖溶液 | 氧化铝 | 二氧化硫 |
C. | 胆矾 | 氢氧化铁胶体 | 铁 | 碳酸钙 |
D. | 水银 | 澄清石灰水 | 氯化铜 | 碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点
(1)氨氮是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,其相关反应的主要热化学方程式如下:
反应①:NH3(aq)+HClO(aq)= NH2Cl(aq)+H2O(l)△H1= akJmol﹣1
反应②:NH2Cl(aq)+HClO(aq)= NHCl2(aq)+H2O(I)△H2= bkJmol﹣1
反应③:2NHCl2(aq)+H2O(l)= N2(g)+HClO(aq)+3HCl(aq)△H3= ckJmol﹣1
① 2NH3(aq)+3HClO(aq)= N2(g)+3H2O(I)+3HCl(aq)的△H=______。
② 溶液pH对次氯酸钠去除氨氮有较大的影响(如图1所示)。在pH较低时溶液中有无色无味的气体生成,氨氮去除效率较低,其原因是_________________。
③ 用电化学法也可以去除废水中氨氮.在蒸馏水中加入硫酸铵用惰性电极直接电解发现氨氮去除效率极低,但在溶液中再加入一定量的氯化钠后,去除效率可以大大提高。反应装置如图2所示,b为电极__极,电解时阴极的电极反应式为_____________。

(2)“低碳经济”正成为科学家研究的主要课题。
① 以二氧化钛表面覆盖Cu2Al2O4 为催化剂,可以将CO2 和CH4 直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如右图所示。250~300 ℃时,温度升高而乙酸的生成速率降低的原因是__________________。
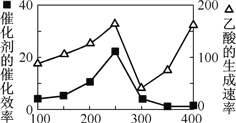
② 为了提高该反应中CO2的转化率,可以采取的措施是_____________。(写一条即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计及其对应的离子方程式均正确的是( )
A. 将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO-
B. 水玻璃在空气中变质:Na2SiO3+CO2+H2O=2Na++CO32-+H2SiO3↓
C. 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+
D. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO![]() +6H++5H2O2=2Mn2++5O2↑+8H2O
+6H++5H2O2=2Mn2++5O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017绍兴模拟】下列关于反应速率的说法错误的是( )
A.反应速率用于衡量化学反应进行的快慢
B.可逆反应达到化学平衡状态时,正、逆反应速率都为0
C.决定反应速率的主要因素是反应物的性质
D.增大反应物浓度,提高反应温度都能增大反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com