
| A. | 碳酸钠溶液呈碱性:CO32-+H2O?HCO3-+OH- | |
| B. | 碳酸溶液呈酸性:H2CO3?2H++CO32- | |
| C. | Cl2溶于水:Cl2+H2O?Cl-+ClO-+2H+ | |
| D. | 往有足量的碳酸镁固体的溶液中加入NaOH固体:Mg2++2OH-═Mg(OH)2(已知:Ksp(Mg(OH)2)>Ksp(MgCO3) |
分析 A.碳酸根离子的水解分步进行,主要以第一步为主;
B.碳酸为二元弱酸,电离方程式分步书写,主要写出第一步电离即可;
C.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
D.碳酸镁为难溶物,离子方程式中不能拆开.
解答 解:A.碳酸钠溶液中碳酸根离子发生水解:CO32-+H2O?HCO3-+OH-,导致溶液呈碱性,故A正确;
B.碳酸溶液中,碳酸的电离方程式主要以第一步为主,正确的电离方程式为:H2CO3?H++HCO3-,故B错误;
C.Cl2与水反应生成氯化氢和次氯酸,正确的离子方程式为:Cl2+H2O?Cl-+ClO-+2H+,故C错误;
D.由于Ksp(Mg(OH)2)<Ksp(MgCO3),往有足量的碳酸镁固体的溶液中加入NaOH固体后,碳酸镁转化成氢氧化镁沉淀,碳酸镁不能拆开,正确的反应为:MgCO3+2OH-═Mg(OH)2+CO32-,故D错误;
故选A.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
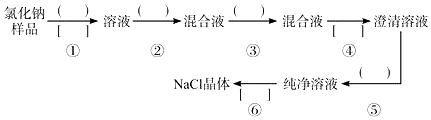
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以选用炭棒作为阴、阳极材料,但阳极材料也可以用铁棒 | |
| B. | 用湿润的淀粉KI试纸靠近阴极区域,试纸变蓝 | |
| C. | 电解过程中,在阴极区域溶液中滴加酚酞,溶液变红色 | |
| D. | 实验结束后将溶液搅拌,然后用pH试纸检验,溶液呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 | |
| B. | 盐酸可作铁制品的除锈剂 | |
| C. | 实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 | |
| D. | 将FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A | 向滴有酚酞的NaOH溶液中通入 Cl2 | 溶液褪色 | HClO有漂白性 |
| B | 无水乙醇与浓硫酸共热至170℃,将产生气体通入溴水 | 溴水褪色 | 乙烯和溴水发生加成反应 |
| C | 向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者红色深 | 结合H+能力: CO32->HCO3- |
| D | 用发光小灯泡分别做HCl和CH3COOH导电性实验 | 发光强度:HCl强于CH3COOH | CH3COOH是弱电解质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有Al3+、Cl-,一定没有HCO3-和SO42- | |
| B. | 肯定有Al3+、Mg2+、Cl-,可能有NH4+、K+ | |
| C. | 肯定有Al3+、NH4+、Cl-,肯定没有HCO3- | |
| D. | 该溶液可能显弱酸性,也可能显中性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com