
| ��� | ���� | ���� | ���� |
| A | ��ʢ�������IJ������м�������ֲ���ͣ���ֽ��衢���� | �ϲ���Һ��ɫ���²���� | ����ɫ����ֲ�����е��ܽ�ȱ���ˮ��С |
| B | ��Ũ�Ⱦ�Ϊ0.1mol/L�Ĵ�����������Һ�зֱ�μӵ�Ũ��Na2CO3��Һ | ǰ�߲����������ݣ����������� | ����ǿ��˳���̼����� |
| C | ��̼����立ֽ����������ͨ��CaC12��Һ | ������ɫ���� | CO2��CaC12��Һ��Ӧ����CaCO3���� |
| D | ���Թ��н�ij�л�����������Һ����� | �������������� | ���л���һ����ȩ������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A�������ܶȱ�ˮС���ϲ���Һ��ɫ���²����ҷ���ɫ���������л��
B��һ����˵��ǿ�����������η�Ӧ�������
C��CO2��CaC12��Һ����Ӧ��
D������������Ӧ�IJ�һ��Ϊȩ�࣬��Ӧ����ȩ����
��� �⣺A�������ܶȱ�ˮС���ϲ���Һ��ɫ���²�����˵������ɫ����ֲ�����е��ܽ�ȱ���ˮ�д�A����
B����������̼���Ʒ�Ӧ��˵���������Դ���̼�ᣬ�����̼���Ʒ�Ӧ��˵����������̼�ᣬ��B��ȷ��
C��CO2��CaC12��Һ����Ӧ��֮�������ɳ���������Ϊ�����Ĵ��ڣ���C����
D������������Ӧ�IJ�һ��Ϊȩ�࣬��Ӧ����ȩ�����������ǵȣ���D����
��ѡB��
���� ���⿼��ʵ�鷽�������ۣ�Ϊ�߿��������ͣ��漰���ʵļ��顢�Ƚϵȣ�������ѧ���ķ���������ʵ�������Ŀ��飬ע�����ʵ��������ԺͿ����Ե����ۣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
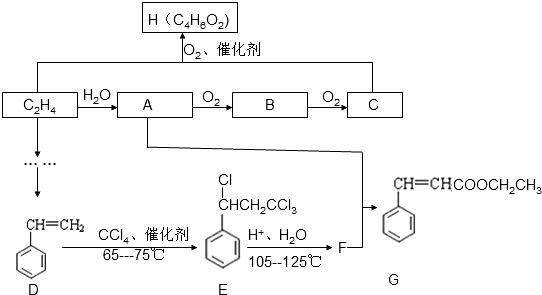
 ��G��һ��ͬ���칹��
��G��һ��ͬ���칹��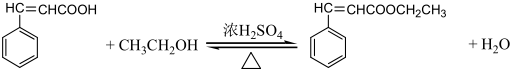 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
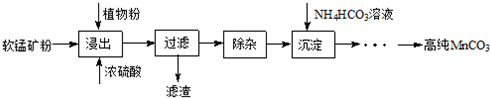
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | ʵ������ | ���� |
| A | ��ʢ��Fe��NO3��2��Һ���Թ��м���0.1mol•L-1 H2SO4��Һ | �Թܿڳ��ֺ���ɫ���� | ��Һ��NO3-��Fe2+��ԭΪNO2 |
| B | ���з�̪��Na2CO3��Һ�м�������BaC12���壬 | ��Һ��ɫ��dz | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
| C | �����pH=2��HX��HY������ֱ�������������Ӧ����ˮ���ռ����� | HX�ų����������ҷ�Ӧ���ʿ� | HX���Ա�HYǿ |
| D | �ֱ�ⶨ�����µ����ʵ���Ũ�ȵ�Na2SO3��Na2CO3��Һ��pH | ���߽ϴ� | ֤���ǽ����� S��C |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
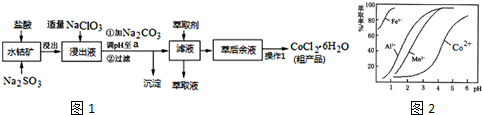
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
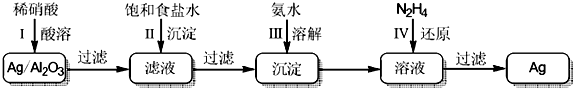
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
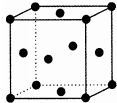 X��Y��Z��R��TΪǰ������Ԫ�أ���ԭ��������������Y��Rͬ�壬Y���⻯�ﳣ����Ϊ��ɫ��ζ��Һ�壬X��Y���γ�ֱ���η���XY2��Z�Ļ�̬ԭ��p����ϵ�������Ϊ7��T2+���ӵ�3d�������3�����ӣ�
X��Y��Z��R��TΪǰ������Ԫ�أ���ԭ��������������Y��Rͬ�壬Y���⻯�ﳣ����Ϊ��ɫ��ζ��Һ�壬X��Y���γ�ֱ���η���XY2��Z�Ļ�̬ԭ��p����ϵ�������Ϊ7��T2+���ӵ�3d�������3�����ӣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
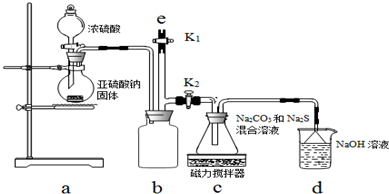
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | �Ҵ���Ӧʱ�ϼ���λ | B | ���ŵ��Ӱ�� |
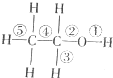 ��1����Ũ���Ṳ�ȵ�170��ʱ�ڢݶϼ� ��2����Ũ���Ṳ�ȵ�140��ʱֻ�ϼ��� | ��1�����Ʒ�Ӧʱ�Ҵ���ˮ����˵�����һ�Ӱ�죬���ǻ���Hԭ�ӻ����Լ��� ��2��������Һ�м�Na0H��Һ����壬˵���ܱ���Ӱ�죬���ǻ���Hԭ�ӻ�������ǿ | ||
| C | �����ᴿ | D | ��������; |
| ��1����ҵ�Ҵ�ͨ���������ˮ�Ҵ� ��2�����л��б��ӣ�����ˮ��������ˣ���ȥ���屽�ӳ��� | ��1�����ͼ�ˮ�������� ��2����������ж�����������ɱ������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com