
| A.二氧化硅可以用来制造光导纤维 | B.工艺师利用盐酸刻蚀石英制作艺术品 |
| C.水晶项链和餐桌上的瓷盘都是硅酸盐制品 | D.粗硅制备单晶硅不涉及氧化还原反应 |
 口算能手系列答案
口算能手系列答案科目:高中化学 来源:不详 题型:填空题
| A.可以利用某些炼钢废渣来生产磷肥 |
| B.具有永久硬度的水主要用加热的方法来进行软化 |
| C.硫酸工业中,在接触室安装热交换器是为了利用S03转化为H2S04时放出的热量 |
| D.合成氨工业原料气净化时,常用碳酸钾溶液吸收除去二氧化碳 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2NaCl(熔融)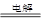 2Na+Cl2↑ 2Na+Cl2↑ | B.MgO+H2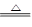 Mg+H2O Mg+H2O |
C.Fe2O3+3CO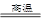 2Fe+3CO2 2Fe+3CO2 | D.2Ag2O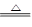 4Ag+O2↑ 4Ag+O2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.增大煤炭燃烧时放出的热量 |
| B.使得燃料燃烧充分,从而提高燃料的利用率 |
| C.增大煤炭与氧气的接触几率,形成清洁能源 |
| D.减少炉中杂质气体(如SO2等)的形成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
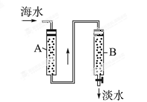
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.凡含有食品添加剂的食物对人体健康均有害,不可食用 |
| B.为防止电池中的重金属和酸碱等污染土壤和水体,应积极开发废电池的回收利用技术 |
| C.当今社会用量最大的合金是镁铝合金 |
| D.工业上用H2还原MgCl2的方法制取金属镁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
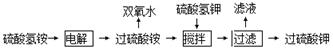

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
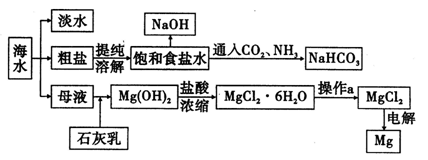
| A.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| B.制铁:以铁矿石为原料,CO还原得铁 |
| C.制镁:用海水为原料,经一系列过程制得氧化镁固体,H2还原得镁 |
| D.制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com