
| A. | 升温 | B. | 使用合适的催化剂 | ||
| C. | 增大压强 | D. | 增大H2O(g)的浓度 |
分析 要提高CO的转化率,应改变条件使平衡向正反应方向移动,结合外界条件对化学平衡移动的影响分析,注意不能得到增大CO的用量,只增大CO的浓度,平衡虽然向正反应方向移动,但CO的转化率降低.
解答 解:A.该反应正反应是放热反应,升高温度,平衡向逆反应方向移动,CO的转化率降低,故A错误;
B.使用催化剂,加快反应速率,不影响平衡移动,CO的转化率不变,故B错误;
C.该反应前后气体的体积不发生变化,增大压强平衡不移动,CO的转化率不变,故C错误;
D.增大水蒸气的浓度,平衡向正反应方向移动,水的转化率降低,但CO的转化率增大,故D正确;
故选D.
点评 本题考查化学平衡的影响因素,比较基础,注意理解外界条件对化学平衡移动的影响.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
 化学平衡mA(g)+nB(g)?pC(g)+qD(g),如图所示是A的转化率同压强,温度的关系,分析图象可以得出的正确结论是( )
化学平衡mA(g)+nB(g)?pC(g)+qD(g),如图所示是A的转化率同压强,温度的关系,分析图象可以得出的正确结论是( )| A. | 正反应吸热,m+n<ρ+q | B. | 正反应吸热,m+n>ρ+q | ||
| C. | 正反应放热,m+n<ρ+q | D. | 正反应放热:m+n>ρ+q |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直径介于1 nm~100 nm之间的微粒称为胶体 | |
| B. | 制备Fe(OH)3胶体的方法是将饱和FeCl3溶液加热煮沸 | |
| C. | 利用丁达尔效应可以区分溶液和胶体 | |
| D. | 溶液、胶体与浊液的本质区别是其稳定性,胶体属于介稳体系 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c (Na+)═c(CH3COO-)+c(CH3COOH) | B. | c(H+)═c(CH3COO-)+c(OH一) | ||
| C. | c (Na+)>c (CH3COO-)>c(OH-)>c(H+) | D. | c (CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .由反应Co2O3+6HCl═2CoCl2+Cl2↑+3H2O可得出,Co2O3氧化性大于Cl2氧化性.
.由反应Co2O3+6HCl═2CoCl2+Cl2↑+3H2O可得出,Co2O3氧化性大于Cl2氧化性.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2a+3b | B. | a+3b | C. | a+3b+7c | D. | 2a+3b+7c |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
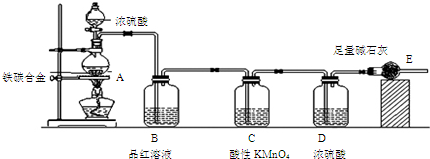
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com