
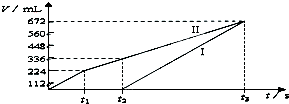
| A、0.1mol/L |
| B、0.15mol/L |
| C、0.2mol/L |
| D、0.25mol/L |
| 0.224L |
| 22.4L/mol |
| 0.02mol |
| 0.2L |
| 0.112L |
| 22.4L/mol |
| 0.04mol |
| 2 |
| 0.02mol |
| 0.2L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时负极反应式为Pb-2e-+SO42-=PbSO4 |
| B、充放电时,溶液的导电能力变化不大 |
| C、以该电池电解NaCl溶液时,当消耗207gPb时,在阳极生成Cl222.4L |
| D、充电时的阳极反应式为Pb 2++2e-+4OH-=PbO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10mx | ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
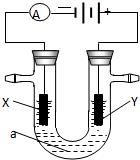 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④ | B、①③ | C、①⑤ | D、③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X是H2O |
| B、还原性:SO42->Mn2+ |
| C、该反应中酸性介质可以为盐酸 |
| D、每生成0.1molSO42-,转移电子0.05mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、SO42-、Br-、SiO32- |
| B、H+、Fe2+、Cl-、NH4+ |
| C、Na+、Ba2+、NO3-、Cl- |
| D、Na+、Ag+、NH3?H2O、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com