
闪锌矿(主要成份为ZnS)是含锌主要矿物之一,高温加热闪锌矿生成ZnO和SO2。ZnO用于冶炼金属锌,SO2可制亚硫酸盐或硫酸。计算回答下列问题(保留2位小数)
(1)取1.56 g闪锌矿样品,在空气中高温加热(杂质不反应),充分反应后,冷却,得到残留固体的质量为1.32 g,样品中含硫化锌的质量分数是_________。
(2)取1.95 g锌加入到12.00 mL 18.4 mol/L的浓硫酸中(假设生成的气体中无氢气,浓硫酸产生单一的还原产物),充分反应后,小心地将溶液稀释到1000 mL,取出15.00 mL,以酚酞为指示剂,用0.25 mol/L的NaOH溶液滴定,耗用NaOH溶液的体积为21.70 mL。通过计算确定浓硫酸被还原的产物是________。
(3)若将ZnS溶于强酸可产生硫化氢气体。在120 oC、1 atm下,将100 mL硫化氢和氧气的混合气体点燃,恢复到原来状态,测得剩余气体为70 mL,求原混合气体中硫化氢的体积分数。(不考虑硫化氢气体自身受热分解)
(4)将标况下4.48 L SO2气体慢慢通入200 mL一定浓度NaOH溶液中,SO2气体全部被吸收,将反应后的溶液在空气中小心蒸干(不考虑酸式盐的分解),得到不超过两种物质的无水晶体26.8g。通过计算确定所得晶体的成分与物质的量。
(1)0.93 (3分)
(2)S (3分)
(3)60%或70% (4分)
(4)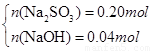
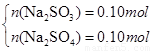
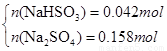
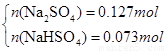 (4分)
(4分)
【解析】
试题分析:(1)解析:设闪锌矿中ZnS的质量为x,杂质为y
2ZnS+3O2=2 ZnO+2SO2
x/97 x/97
有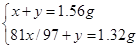
解得x=1.455g,y=0.105g,所以样品中w(ZnS)=1.455g÷1.56g×100%=93%
(2)解析:设浓硫酸被还原的产物中S的化合价为x。
根据题意过量的硫酸用碱滴定,则过量的硫酸n(H2SO4)= n(NaOH)×1000/15=0.25 mol/L×0.02170 L×1000/15=0.1808mol,所以反应的硫酸n(H2SO4)=18.4 mol/L×0.012L-0.1808mol=0.04mol,又反应后溶液为硫酸锌,所以n(ZnSO4)= n(Zn)=1.95 g÷65g/mol=0.03mol,所以作酸的硫酸n(H2SO4)= n(ZnSO4)=0.03mol,做氧化剂硫酸n(H2SO4)=0.04mol-0.03mol=0.01mol,因为Zn反应0.03mol失去0.06mol电子,所以根据得失电子守恒,(+6-x) ×0.01mol=0.06mol,解得x=0,所以还原产物中S的化合价为0价,还原产物为S单质。
(3)解析:在120 oC、1 atm下,设硫化氢和氧气体积分别为x、y,点燃生成的都是气态产物,由于比例不定,
所以若氧气过量,则有:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g)
2 3 2 2
x y x x
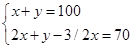
解得x=60ml,y=40ml;所以此时硫化氢的百分数为60ml÷100ml×100%=60%
若硫化氢过量,则有:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g)
2 3 2 2
x y 2/3y 2/3y

解得x=10ml,y=90ml;此时得到数据不满足条件舍去。
(4)解析:n(SO2)=0.2mol,通入未知浓度的NaOH溶液,若NaOH溶液过量则所得溶液为Na2SO3 、NaOH;若恰好完全反应则所的溶液为Na2SO3 溶液;若SO2稍过量则所得溶液为Na2SO3 、NaHSO3 ;若SO2过量恰好完全被吸收则生成NaHSO3 溶液;
(1)若所得溶液为Na2SO3 、NaOH:则有n(Na2SO3)= n(SO2)=0.2mol,则m(Na2SO3)=25.2g<26.8g,
蒸干后若得到的是Na2SO3 、NaOH时,满足条件,此时m(NaOH)= 26.8g-25.2g=1.6g,即n(NaOH)=0.04mol.
(2)若恰好完全反应所得溶液为Na2SO3 :因n(Na2SO3)= n(SO2)=0.2mol,则m(Na2SO3)=25.2g<26.8g,蒸干后必有部分Na2SO3 被氧化为Na2SO4 ;设n(Na2SO3)=x,n(Na2SO4)=y,则有:
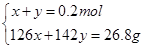
解得x=0.1mol,y=0.1mol即n(Na2SO3)=0.1mol,n(Na2SO4)= 0.1mol.
(3)若SO2稍过量所得溶液为Na2SO3 、NaHSO3 :当蒸干后固体全为Na2SO3时,m(Na2SO3)=25.2g<26.8g,所以蒸干溶液后所得晶体不可能是Na2SO3 、NaHSO3 组合;当蒸干后固体全为Na2SO4 时,m(Na2SO4)=0.2mol×142g/mol=28.4g >26.8g,所以蒸干后不可能全是Na2SO4,可以是Na2SO4 和NaHSO3或者是Na2SO4 和NaHSO4 ,因此有
设n(NaHSO3)=x,n(Na2SO4)=y
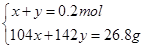
解得x=0.042mol,y=0.158mol即n(NaHSO3)= 0.042mol,n(Na2SO4)= 0.158mol
设n(NaHSO4)=x,n(Na2SO4)=y
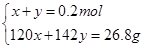
解得x=0.073mol,y=0.127mol即n(NaHSO3)= 0.073mol,n(Na2SO4)= 0.127mol
(4)若SO2过量恰好被吸收所得溶液为NaHSO3 :则蒸干后所得固体无论是NaHSO3 还是NaHSO4 或者二者混合,都不可能。
考点:本题考查的是氧化还原计算、金属与酸反应计算、多元酸的酸性氧化物与碱反应的计算。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源:江苏省南海中学2008届高三化学第一次月考试题 题型:022
某地有软锰矿(主要成份为MnO2,含少量Al2O3、SiO2)和闪锌矿(主要成份ZnS,含少量FeS、CuS、CdS、SiO2),科研人员采用新工艺生产二氧化锰和锌,同时还得副产品镉和X、Y、Z等.工业流程图如下图(框图中水省略):

请回答:
(1)Y的名称是________、Z的化学式为________.
(2)他们的主要产品中的元素在周期表中,锌属________族,X在________周期.
(3)图中“操作(1)~(4)”都包含的共同一种操作,在实验室中该操作的名称为________.
(4)操作(1)中,在稀H2SO4存在下MnO2把硫化物氧化成硫单质和+2价硫酸盐.如果硫化物用MS表示,请写出MnO2与硫化物反应的化学方程式:__________.
(5)旧工艺生产二氧化锰,是将软锰矿与煤混合粉碎后高温焙烧,再用硫酸浸取焙烧料净化后电解.对比旧工艺,新工艺有好多个优点,请你至少说出新工艺的一个优点:_______________________________.
查看答案和解析>>
科目:高中化学 来源:2007高州中学高三化学每周一练(3) 题型:022
| |||||||||||||||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com