
分析 (1)根据配制一定物质的量浓度的溶液的步骤是:计算、称量、溶解、移液、洗涤、定容、摇匀来选择使用的仪器;根据使用玻璃棒的操作来分析其用途;
(2)配制溶液的最后必须倒转过来摇匀,此操作要求容量瓶不能漏水;
(3)据配制溶液的实验操作过程进行实验步骤排序.
解答 解:(1)根据配制一定物质的量浓度的溶液的步骤是:计算、称量、溶解、移液、洗涤、定容、摇匀可知需要的仪器有:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶和胶头滴管,故必须使用的仪器有:①②④⑤⑥⑥⑦,还缺少的仪器室胶头滴管;
在配制过程中,溶解氢氧化钠固体时玻璃棒的用途是:搅拌,加速溶解;在移液时玻璃棒的用途是引流,
故答案为:①②④⑤⑥⑦;胶头滴管;搅拌、加速溶解;引流;
(2)配制溶液的最后必须倒转过来摇匀,此操作要求容量瓶不能漏水,故容量瓶在使用前必须查漏,
故答案为:检查是否漏水;
(3)配制0.5mol•L-1的NaOH溶液500mL,配制步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,用天平称量NaOH(用到药匙),在烧杯中稀释,并用玻璃棒搅拌,加速溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,并将洗涤液移入容量瓶,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以操作顺序是②①③⑧⑤⑥⑦④.
故答案为:②①③⑧⑤⑥⑦④.
点评 本题考查了一定物质的量浓度溶液的配制过程中涉及到的仪器的选择和使用等问题,属于基础型题目,题目难度不大.


科目:高中化学 来源: 题型:解答题
 Ω=4;⑤
Ω=4;⑤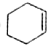 Ω=2;⑥
Ω=2;⑥ Ω=4.
Ω=4.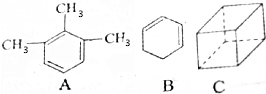
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
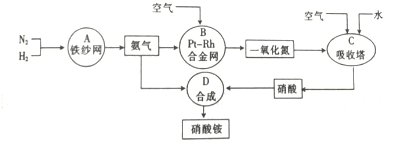
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
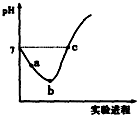 常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )| A. | 实验进程中可用pH试纸测定溶液的pH | |
| B. | a点的溶液中:c(H+)=c(Cl-)+c(HClO)+c(OH-) | |
| C. | 由a点到b点的过程中,溶液中C(H+):C(ClO-)减小 | |
| D. | c点所示溶液中:c(Na+)=2c(ClO-)+c(HClO) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,a个-CH 3,其余为-OH,则该物质分子中-OH的个数可能为( )
,a个-CH 3,其余为-OH,则该物质分子中-OH的个数可能为( )| A. | m-a | B. | n+m+a | C. | m+1-a | D. | m-1-a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X极为负极,Y极为正极 | |
| B. | 工作一段时间后,KOH的物质的量不变 | |
| C. | 电池工作时甲烷一极附近溶液的pH减小 | |
| D. | 该在标准状况下通入5.6 L O2完全反应,则有1.0mol电子发生转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用作荧光灯内壁保护层的氧化铝纳米材料属于胶体 | |
| B. | 高分子材料可能导电,如聚乙炔 | |
| C. | 钢化玻璃、有机玻璃、防弹玻璃均属于硅酸盐材料 | |
| D. | 人造刚玉的主要成分是MgO,熔点很高,可用作高级耐火材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com