
 C2H4(g)�� �� CH4(g)
C2H4(g)�� �� CH4(g)  H2(g) + C2H4(g)��
H2(g) + C2H4(g)�� CH4(g)����H����x KJ�� mol��1��
CH4(g)����H����x KJ�� mol��1�� 1/2C2H2(g)����H����y KJ�� mol��1��
1/2C2H2(g)����H����y KJ�� mol��1��| A��x >y>z | B��x>z>y | C��y>x>z | D��z |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
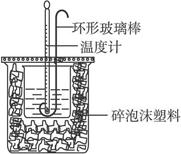
| ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | |
| ���� | NaOH��Һ | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ʽ̼��ͭ | B��ˮ |
| C�������� | D��̼�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ȷ�Ӧ��������������һ�����ڷ�Ӧ�������� |
| B�����ȷ�Ӧ�ķ�Ӧ�������Ǵ������ȷ�Ӧ�ķ�Ӧ���� |
| C����˹����ʵ�����������غ㶨�ɵ����� |
| D������ƽ�⡢ˮ��ƽ��ͳ����ܽ�ƽ���Ϊ��̬ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ֲ�������ã����� �� �������� | B����ʯȼ��ȼ�գ���ѧ�� �� ���� |
| C�����ʳ��ˮ����ѧ�� �� ���� | D��̫������ˮ��ʹ�ã����� �� ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
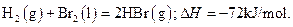 ����1mol Br2��l����Ҫ���յ�����Ϊ30kJ����������������±���
����1mol Br2��l����Ҫ���յ�����Ϊ30kJ����������������±���
| A��404 | B��260 | C��230 | D��200 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ˮ������Ϊˮ�ų����� | B��ϡ��Ũ���� |
| C����ʯ����ˮ��Ӧ | D������طֽ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ѧ��Ӧ��Ȼ���淢�������仯 |
| B����ѧ�仯�е������仯��Ҫ���ɻ�ѧ���仯����� |
| C����Ӧ�����Ǽ��Ȼ���µķ�Ӧһ�������ȷ�Ӧ |
| D����Ӧ��������������������������ʱ����Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��2H2��g��+O2��g�� ="=" 2H2O(1)��H�� �D285��8kJ��mol |
| B��2H2��g��+ O2��g�� ="=" 2H2O(1)��H�� +571��6 kJ��mol |
| C��2H2��g��+O2��g�� ="=" 2H2O��g����H�� �D571��6 kJ��mol |
| D��H2��g��+O2��g�� ="=" H2O(1)��H�� �D285��8kJ��mol |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com