
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。已知:2Fe2++Br2===2Fe3++2Br-,2Fe3++2I-===2Fe2++I2。则下列有关说法中,不正确的是( )

A.还原性:I->Fe2+>Br-
B.原混合溶液中FeBr2的物质的量为6mol
C.当通入2mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-2·1·c·n·j·y
D.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数,下列说法不正确的是 ( )
A.标准状况下,11.2L氯仿(CHCl3)中含有C-Cl键的数目为1.5NA
B.常温常压下,17g甲基(-14CH3)所含的电子数为9NA
C.同温同压下,1L NO和1L O2充分混合体积小于1.5L
D.pH=l的醋酸溶液100mL中氢离子数为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列叙述正确的是( )
A.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
B.2 L0.5 mol • L-1硫酸钾溶液中阴离子所带电荷数为NA
C.1 mol Na2O2固体中含离子总数为4NA
D. 5NH4NO3 2HNO3+4N2↑+9H2O反应中,生成28 gN2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 gN2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是( )
A.浓盐酸与铁屑反应:2Fe+6H+===2Fe3++3H2↑
B.钠与CuSO4溶液反应:2Na+Cu2+===Cu↓+2Na+
C.NaHCO3溶液与稀H2SO4反应:CO +2H+===H2O+CO2↑
+2H+===H2O+CO2↑
D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+===2Fe(OH)3+3Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
大气中SO2和NOx是形成酸雨的主要物质。某地酸雨中可能含有下列离子:Na+、Mg2+、NH 、Cl-、SO
、Cl-、SO 、SO
、SO 、NO
、NO 和NO
和NO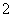 等。某研究小组取该地一定量的酸雨,浓缩后将所得试液分成4份,进行如下实验:第一份酸化后滴加适量的淀粉KI溶液,呈蓝色;第二份滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出;第三份滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝;第四份加入硝酸酸化的AgNO3溶液,有沉淀产生,静置,在上层清液中滴加酸性KMnO4溶液,不褪色。21教育网
等。某研究小组取该地一定量的酸雨,浓缩后将所得试液分成4份,进行如下实验:第一份酸化后滴加适量的淀粉KI溶液,呈蓝色;第二份滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出;第三份滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝;第四份加入硝酸酸化的AgNO3溶液,有沉淀产生,静置,在上层清液中滴加酸性KMnO4溶液,不褪色。21教育网
[已知:Ksp(Ag2SO4)=1.20×10-5]
请回答下列问题:
(1)该酸雨中肯定存在的离子有 SO 、NO
、NO 、NH
、NH ;肯定不存在的离子有 SO
;肯定不存在的离子有 SO 、NO
、NO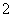 ,说明其不存在的理由:________________________________________________________________________
,说明其不存在的理由:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)写出试液中滴加淀粉KI溶液所发生反应的离子方程式:________________________________________________________________________
________________________________________________________________________。
(3)设计实验方案,检验该试液中是否存在Cl-:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(4)该研究小组为了探究NO参与的硫酸型酸雨的形成,在烧瓶中充入含有少量NO的SO2气体,慢慢通入O2,该过程中发生的化学反应有________________________________________________________________________、
________________________________________________________________________,
再喷射适量蒸馏水即得硫酸型酸雨。说明NO的作用: 催化剂 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某一反应体系中的物质有HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,其中As是产物之一:
(1)写出并配平该反应的化学方程式:________________________________________________________________________
________________________________________________________________________。
(2)在该反应中,得电子的物质是 H3AsO3 (填化学式),被氧化的元素是 Sn (填元素符号)。
(3)在该反应中,每转移1 mol电子,消耗(生成)HCl 2 mol。
(4)下列叙述正确的是 AC (填序号)。
A.在相同条件下,ⅦA族元素阴离子的还原性从上到下逐渐增强
B.Sn和Pb位于同一主族,其+4价的化合物均很稳定
C.在相同条件下,还原性顺序为S2->I->Fe2+>Br->Cl-
D.在上述反应中,氧化性SnCl2>As,还原性H3AsO3>H2SnCl6
查看答案和解析>>
科目:高中化学 来源: 题型:
已知CH3CH2Br+2Na+CH3CH2Br CH3CH2CH2CH3+2NaBr。下列有机物发生这种反应可生成X,若X与环丙烷互为同系物,则能生成X的是( )
CH3CH2CH2CH3+2NaBr。下列有机物发生这种反应可生成X,若X与环丙烷互为同系物,则能生成X的是( )
A.CH3CH2CH2Cl B.CH3CHBrCH(CH3)CH2Br
C.CH3CHBrCH2CH2Br D.CH3CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
| C | ||
| B |
右图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是( )
A B为第二周期的元素 C 三种元素都为金属元素
B C为VA族元素 D C是化学性质最活泼的非金属
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质属于强电解质且能导电的是
①氯化钠溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融NaOH ⑥稀硫酸 ⑦乙酸
A.⑤ B.①②⑥
C.②⑤⑥⑦ D.①③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com