
(10分)固定和利用CO2能有效地利用资源,并减少空气中的温室气体.工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.
CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.
(1)0~a,a~b,b~c,c~d四段中,平均反应速率最大的时间段是___________ ,该时间段内H2的平均反应速率是_____________。
(2)平衡时CO2的转化率是多少?反应前后容器内的压强比时多少?(请按计算题格式在答题卡上作答)
L)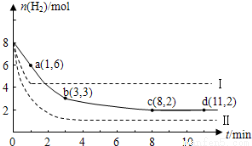
(1)0~a段;该时间段内H2的平均反应速率是1mol/(L·min) (2)33% ;7︰5
【解析】
试题分析:(1)0~a段:V(H2)=(8mol-6mol)÷2L÷1min=1mol/(L·min); a~b段:V(H2)=(6mol-3mol)÷ 2L÷ 2min=0.75mol/(L·min); b~c段:V(H2)=(3mol-2mol)÷2L÷5min=0.1mol/(L·min); c~d段:V(H2)=(2 mol- 2mol)÷2L÷5min0=0.1mol/(L·min)。所以平均反应速率最大的时间段是0~a段。该时间段内H2的平均反应速率是1mol/(L·min)。(2) 在反应过程中H2的物质的量改变6mol,因为CO2与H2反应的物质的量的比为1:3,所以CO2反应消耗的物质的量为2mol.因此平衡时CO2的转化率是(2mol÷6molCO2) ×100%= 33%。反应前后容器内的压强比等于气体的物质的量的比。在反应开始时,n(总)=6+8=14mol;当反应达到平衡时,n(H2)=2mol;n(CO2)=(6-2)mol=4mol;n(CH3OH)=2mol;n(H2O)= 2mol。所以n(总)平衡=10mol.n(开始):n(平衡)=14:10=7︰5。所以反应前后容器内的压强比7︰5。
考点:考查气体的物质的量与压强的关系、化学反应速率的比较与计算及物质的平衡转化率的计算的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014甘肃省第二学期第一学段段中检测化学试卷(解析版) 题型:填空题
(1)(3分)通过实验事实的验证与讨论,认识苯的结构式。提出问题:苯分子结构是碳碳单双键交替的环状结构吗?
①提出假设:从苯的分子式看,C6H6具有不饱和性;从苯的凯库勒结构式看,分子中含有碳碳双键,但实验验证:苯不能使 褪色;
②经科学测定,苯分子里6个碳原子之间的键 (相同或不同);6个碳原子和6个氢原子都在同一平面上。
③应用:为了表示苯分子的结构特点,可用 来表示苯分子的结构式,而凯库勒式表示苯分子结构式是不确切的,只是人们沿用至今。
(2)(10分)乙醇的分子式 ,电子式 ,结构简式 ,官能团为 ,官能团名称是
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省下学期期中考试高二化学试卷(解析版) 题型:简答题
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
元素 | 相关信息 |
X | X的最高价氧化物对应的水化物化学式为H2XO3 |
Y | Y是地壳中含量最高的元素 |
Z | Z的基态原子最外层电子排布式为3s23p1 |
W | W的一种核素的质量数为28,中子数为14 |
T | 常温常压下,T单质是淡黄色固体,常在火山口附近沉积 |
P | P的价层电子排布为[Ar]3d104s2 |
(1)W位于元素周期表第________周期第________族;W的原子半径比X的________(填“大”或“小”)。
(2)TY2中心原子的杂化方式为_______;XY2中一个分子周围有__________个紧邻分子;堆积方式与XY2晶胞类型相同的金属有_________(从“Cu、 Mg、K、Po”中选出正确的),其空间利用率为_______。
(3)Z的第一电离能比Mg的________(填“大”或“小”);写出Z单质与NaOH溶液反应的化学方程式 。
(4)写出W的最高价氧化物与NaOH溶液反应的离子方程式 ;W的最高价氧化物与XY2的熔点较高的是 ,原因是 。
(5)处理含XO、TO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质T。已知:
① XO(g)+ 1/2O2(g)=XO2(g) ΔH=-283.0 kJ·mol-1 ② T(s)+O2(g)=TO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是______________________________。
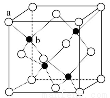
(6)P在周期表的 区;P和T形成的化合物PT在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方PT晶体结构如下图所示,其晶胞边长为540.0 pm,密度为_________ g·cm-3(列式并计算)。
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省下学期期中考试高二化学试卷(解析版) 题型:选择题
下列各项比较中前者高于(或大于或强于)后者的是
A、CCl4和SiCl4的熔点
B、邻羟基苯甲醛( )和对羟基苯甲醛(
)和对羟基苯甲醛(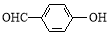 )的沸点
)的沸点
C、SO2和CO2在水中的溶解度
D、H2SO3和H2SO4的酸性
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省下学期期中考试高二化学试卷(解析版) 题型:选择题
下列事实与氢键有关的是
A、HF、HCl、HBr、HI的热稳定性依次减弱
B、水加热到很高的温度都难以分解
C、CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
D、水结成冰体积膨胀
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省下学期期中考试高一化学试卷(解析版) 题型:选择题
在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,,有关物质X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )

A.该反应的化学方程式为: 3Z = 3X+2Y
B.t0时,X、Y、Z的质量不再改变
C.t0时,Z的浓度为1.2 mol/L
D.t0时,反应停止,反应速率为0
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省下学期期中考试高一化学试卷(解析版) 题型:选择题
可逆反应H2(g)+I2(g)  2HI(g)在密闭容器中反应,达到平衡状态时的标志是( )
2HI(g)在密闭容器中反应,达到平衡状态时的标志是( )
A.混合气体的密度不再改变B. 混合气体的颜色不再改变
C.混合气体的压强不再改变D. I2、H2在混合气体中的体积分数相等
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃兰州一中高一下学期期末考试化学试卷(解析版) 题型:选择题
a mL三种气态烃组成的混合物与足量氧气混合,点燃爆炸后,恢复到原来的状态(常温、常压),体积共缩小2a mL。则三种烃可能是
A.CH4、C2H4、C3H4 B.C2H6、C3H6、C4H6
C.CH4、C2H6、C3H8 D.C2H4、C2H2、CH4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com