
����Ŀ�����жԻ�ѧƽ���ƶ��ķ����У�����ȷ���ǣ� ��
���Ѵ�ƽ��ķ�ӦC��s��+H2O��g��![]() CO��g��+H2��g���������ӷ�Ӧ�����ʵ���ʱ��ƽ��һ��������Ӧ�����ƶ�
CO��g��+H2��g���������ӷ�Ӧ�����ʵ���ʱ��ƽ��һ��������Ӧ�����ƶ�
���Ѵ�ƽ��ķ�ӦN2��g��+3H2��g��![]() 2NH3��g����������N2��Ũ��ʱ��ƽ��������Ӧ�����ƶ���N2��ת����һ������
2NH3��g����������N2��Ũ��ʱ��ƽ��������Ӧ�����ƶ���N2��ת����һ������
��������μӵķ�Ӧƽ��ʱ������С��Ӧ���ݻ�ʱ��ƽ��һ���������������ķ����ƶ�
��������μӵķ�Ӧ��ƽ��ʱ���ں�ѹ��Ӧ���г���ϡ�����壬ƽ��һ�����ƶ�
A. �٢� B. �٢ڢ�
C. �ڢۢ� D. �٢ڢۢ�
���𰸡�D
��������������������������ӹ��巴Ӧ��C��������ƽ�ⲻ���ƶ�����Ϊ�������ʵ�Ũ���Dz�������������C��Ũ�ȣ�����������������������ʱ����������Ũ�ȣ�ƽ�������ƶ�����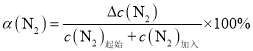 ��֪����Ȼ�����ı仯Ũ����������������ʼŨ��+���ӵ�Ũ������ij̶ȸ���N2��ת���ʷ������С��������ת���ʲ�һ������������������������������ֲ���Ŀ��淴Ӧ����С�ݻ�������ѹǿʱ��ƽ�ⲻһ�����������������ڷ�Ӧǰ����������仯���Ѵ�ƽ��ķ�Ӧ����ѹ��Ӧ���г���ϡ�����壬�ͱ��������ݻ���ʵ�����Ǽ�Сѹǿ��ƽ������������������ƶ���������ѡD��
��֪����Ȼ�����ı仯Ũ����������������ʼŨ��+���ӵ�Ũ������ij̶ȸ���N2��ת���ʷ������С��������ת���ʲ�һ������������������������������ֲ���Ŀ��淴Ӧ����С�ݻ�������ѹǿʱ��ƽ�ⲻһ�����������������ڷ�Ӧǰ����������仯���Ѵ�ƽ��ķ�Ӧ����ѹ��Ӧ���г���ϡ�����壬�ͱ��������ݻ���ʵ�����Ǽ�Сѹǿ��ƽ������������������ƶ���������ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ҩƷ������Ȼҩ������� ��
A����˾ƥ�� B����ù�� C������ҩ D����Ƽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����У�û�з���������ԭ��Ӧ����(����)
A. ��ľȡ�� B. ��ͭ������
C. ȼ���̻����� D. ������ɫ��Ӧ����Na��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ҩ��ҩ���������� ��
A���к�θ�� B������θ����� C���ٽ�ѪҺѭ�� D����к
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�ٽ��Ϸ�����(��Ҫ�ɷ�V2O5)��ϡ���ᡢ���������Һ��ϣ���ַ�Ӧ��������Һ�����ԣ���VO2����K����SO![]() �ȡ�д���÷�Ӧ�Ļ�ѧ����ʽ_______________________��
�ȡ�д���÷�Ӧ�Ļ�ѧ����ʽ_______________________��
��������������Һ�м���KClO3��Һ����ַ�Ӧ����Һ����������VO![]() ��Cl����д������ƽ�÷�Ӧ�����ӷ���ʽ�����������ת�Ƶ���Ŀ�ͷ���____________________��
��Cl����д������ƽ�÷�Ӧ�����ӷ���ʽ�����������ת�Ƶ���Ŀ�ͷ���____________________��
(2)�����������£�����NO![]() ��Ӧ�����ӷ���ʽ����������
��Ӧ�����ӷ���ʽ����������
![]() Fe��
Fe��![]() NO
NO![]() ��
��![]() ________===
________===![]() Fe2����
Fe2����![]() NH
NH![]() ��
��![]() ________
________
(3)���۸�[Cr(��)]�о綾����ˮ�е�Cr2O![]() �����������巨��ȥ�����ѹ�����FeSO4��7H2O���뺬Cr2O
�����������巨��ȥ�����ѹ�����FeSO4��7H2O���뺬Cr2O![]() �ķ�ˮ�У�����pH<4��Fe2����Cr(��)��ԭΪCr3����
�ķ�ˮ�У�����pH<4��Fe2����Cr(��)��ԭΪCr3����
д������Fe2����ԭCr2O![]() �����ӷ���ʽ������������ת�Ƶķ������Ŀ��_________________________��
�����ӷ���ʽ������������ת�Ƶķ������Ŀ��_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�к��е����ӿ�����K����Ba2����Al3����Mg2����AlO![]() ��CO
��CO![]() ��SiO
��SiO![]() ��Cl���еļ��֣��ֽ�������ʵ�飺
��Cl���еļ��֣��ֽ�������ʵ�飺
��ȡ������Һ��������������Һ�������������ɣ�
����ȡ����ԭ��Һ����μ���5 mL 0.2 mol��L��1���ᣬ�����������ǣ���ʼ���������������࣬���������������������壬��������������ʧ��
���������ڳ�����ʧ�����Һ�У��ټ�����������������Һ�ɵõ�����0.43 g��
����˵������ȷ����( )
A������Һ��һ������Ba2����Mg2����Al3����SiO![]() ��Cl��
��Cl��
B������Һ��һ������K����AlO![]() ��CO
��CO![]() ��Cl��
��Cl��
C������Һ�Ƿ���K��������ɫ��Ӧʵ��(����ɫ�ܲ���Ƭ)
D�����ܺ���Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʴ���������ձ������ ��
A����ѧ��ʴ B�����ⸯʴ C��������ʴ D�� Ħ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��ɫ��Һ�����ܺ���K����Al3����Mg2����NH![]() ��Cl����SO
��Cl����SO![]() ��HCO
��HCO![]() ��MnO
��MnO![]() �еļ��֡�Ϊȷ����ɷ֣�������ʵ�飺
�еļ��֡�Ϊȷ����ɷ֣�������ʵ�飺
��ȡ������Һ����������Na2O2���壬������ɫ��ζ������Ͱ�ɫ�������ټ���������NaOH��Һ���ɫ���������ܽ⣻����ȡ������Һ������HNO3�ữ��Ba(NO3)2��Һ���а�ɫ����������
�����ƶ���ȷ����( )
A���϶���Al3����Mg2����NH![]() ��Cl��
��Cl��
B���϶���Al3����Mg2����HCO![]()
C���϶���K����HCO![]() ��MnO
��MnO![]()
D���϶���Al3����Mg2����SO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�������Ӧ��FeO��s��+CO��g��![]() Fe��s��+CO2��g�� ��H����֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����±���
Fe��s��+CO2��g�� ��H����֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����±���
�¶�/�� | 1000 | 1100 |
ƽ�ⳣ�� | 0.68 | 0.50 |
��ش��������⣺
��1���÷�Ӧ�Ħ�H 0
��2��T��ʱ����FeO��s����CO��g����3.0mol����10L���ܱ������У���Ӧ�ﵽƽ����COת����Ϊ��1��c��CO2����0.15molL��1�����¶�T ������ڡ����ڡ�������1000������ʱ�����������������ٳ���2.0 mol CO��g�����ٴ�ƽ��ʱ���COת����2�����1 ��2�������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com