
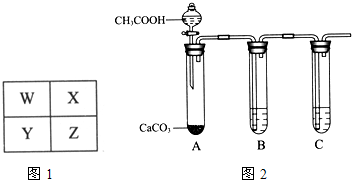
 W、X、Y、Z为四种短周期主族元素,其位置关系如图1.
W、X、Y、Z为四种短周期主族元素,其位置关系如图1.
| ||
| 高温高压 |
| ||
| 高温高压 |
| ||
| 冰晶石 |
| ||
| 冰晶石 |
| ||
| ||


科目:高中化学 来源: 题型:
(1)X的原子结构示意图为__________________。
(2)XY2与Z2Y2反应的化学方程式____________________________________。
(3)W、Y、Z三种元素可组成一种离子化合物,其中阳离子所含电子数与阴离子所含电子数之比为___________________________。
查看答案和解析>>
科目:高中化学 来源:2014届吉林省高一下学期期末考试化学试卷(解析版) 题型:推断题
已知W、X、Y、Z为四种短周期元素,原子序数逐渐增大。其中W形成的单质是自然界中最轻的气体;X原子的最外层电子数是次外层电子数的2倍;Y元素是地壳中含量最多的元素;Z元素是短周期中原子半径最大的元素。回答下列问题:
(1)X6W6的结构简式为 ,分子空间构型为 。
(2)Y与Z形成的两种常见化合物的电子式分别为 和
(3)由W、X、Y三种元素形成的最简式为XW2Y的化合物有A和B两种,其中A的相对分子质量是60,是日常生活中的一种调味品的主要成分,则A的结构简式为 ;B的相对分子质量是A的3倍,在正常人的血液里含有0.1%的B,则B的分子式 。将B物质的溶液与新制的Cu(OH)2悬浊液共热,观察到得现象是 。
(4)将B在酒化酶的作用下可制得另外一种具有特殊香味的液态有机物C,同时得到一种能导致温室效应的气体。写出该反应的化学方程式
(5)C是一种可以再生的清洁燃料,写出其燃烧的化学方程式
。C还可以在Cu或Ag的催化作用下被氧气氧化成具有刺激性气味的液体,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2010年黑龙江省五大连池市等五校联谊高一下学期期末考试 题型:填空题
(13分)已知W、X、Y、Z为四种短周期元素,原子序数逐渐增大。其中W形成的单质是自然界中最轻的气体;X原子的最外层电子数是次外层电子数 的2倍;元素是地壳中含量最多的元素;Z元素是短周期中原子半径最大的元素。回答下列问题:
的2倍;元素是地壳中含量最多的元素;Z元素是短周期中原子半径最大的元素。回答下列问题:
 (1)X6W6的结构简式为 ,分子空间构型为
。
(1)X6W6的结构简式为 ,分子空间构型为
。
(2)Y与Z形成的两种常见化合物的电子式分别为 和
 (3)由W、X、Y三种元素形成的最简式为XW2Y的化合物有A和B两种,
(3)由W、X、Y三种元素形成的最简式为XW2Y的化合物有A和B两种,
其中A的相对分子质量是60,是日常生活中的一种调味品的主要 成分,则A的结构简式为 ;B的相对分子质量是A的3倍,在正常人的血液里含有0.1%的B,则B的分子式 。
成分,则A的结构简式为 ;B的相对分子质量是A的3倍,在正常人的血液里含有0.1%的B,则B的分子式 。 将B物质的溶液与新制的Cu(OH)2悬浊液共热,观察到得现象是
。
将B物质的溶液与新制的Cu(OH)2悬浊液共热,观察到得现象是
。
 (4)将B在酒化酶的作用下可制得另外一种具有特殊香味的液态有机物C,同时得到一种能导致温室效应的气体。写出该反应的化学
(4)将B在酒化酶的作用下可制得另外一种具有特殊香味的液态有机物C,同时得到一种能导致温室效应的气体。写出该反应的化学 方程式
方程式
(5)C是一种可以再生的清洁燃料,写出其燃烧的化学方程式
 。
。
C还可以在Cu或Ag的催化作用下被氧气氧化成具有刺激性气味的液体,该反应的化学方程式为  。
。




查看答案和解析>>
科目:高中化学 来源:2013届辽宁大连23中高一下学期期末考试化学试卷 题型:选择题
W、X、Y、Z为四种短周期元素,X、Z同主族。已知X的原子半径大于Z的原子半径;Y的阳离子比W的阳离子氧化性强;Y的阳离子、W的阳离子、Z的阴离子具有相同的电子层结构。下列叙述正确的是
A.原子半径:W>X >Y>Z
B.单质与盐酸反应速率:Y>W
C.X最低价氢化物的稳定性强于Z最低价氢化物
D.W的氢氧化物的碱性强于Y的氢氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com