【答案】
分析:方法一中将天青石粉碎的目的是增加反应物的接触面积,提高化学反应速率和原料的利用率,碳还原天青石的化学方程式为4C+SrSO
4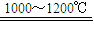
SrS+4CO↑;
方法二是利用碳酸锶的溶解度小于硫酸锶,溶解沉淀平衡向离子减少的方向进行的原理,在反应过程中不断搅拌可以提高反应的速率和效率;方法二的最大缺点是不能及时除去碳酸锶中的不溶性杂质;
根据元素周期律的递变规律解答,结合物质性质的相似性和递变性解答该题.
解答:解:(1)增大表面积,使之与碳粒能够充分接触,充分反应,发生:4C+SrSO
4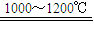
SrS+4CO↑,
因为要保证还原气氛,所以产物是CO而不是CO
2,
故答案为:增加反应物接触面积,提高反应速率和原料的利用率;4C+SrSO
4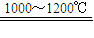
SrS+4CO↑;
(2)沉淀转化的实质是溶解平衡的移动,将天青石粉末与碳酸钠溶液的混合物在90℃时加热1~2h,经过滤、洗涤,得到碳酸锶,说明碳酸锶的溶解度小于硫酸锶的溶解度,在反应过程中不断搅拌可以提高反应的速率和效率
故答案为:碳酸锶的溶解度小于硫酸锶的溶解度;搅拌;
(3)天青石中含有不溶性杂质,而方法二的最大缺点是不能及时除去碳酸锶中的不溶性杂质,方法一通过过滤可以除去不溶性杂质,故答案为:方法一;硫化锶可溶于水,通过过滤可以除去不溶性杂质;
(4)A、同主族元素从上到下离子半径逐渐增大,故A正确;
B、同主族元素从上到下元素的金属性逐渐增强,对应的最高价氧化物的水合物的碱性逐渐增强,故B正确;
C、碳酸盐不稳定,在高温下可分解生成对应的金属氧化物和二氧化碳,故C正确;
D、碳酸盐可与硝酸发生复分解反应,生成Sr(NO
3)
2,故D正确,
故答案为:ABCD.
点评:本题考查同一主族元素的性质,题目难度中等,注意通过同主族元素的相似性,将不熟悉的锶看作较为熟悉的钙进行分析、思考,是解答本题的有效途径之一.

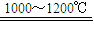 SrS+4CO↑;
SrS+4CO↑;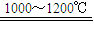 SrS+4CO↑,
SrS+4CO↑,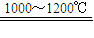 SrS+4CO↑;
SrS+4CO↑;
