
 �� (4)9
�� (4)9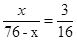 �����x��12������Y�����ԭ��������32����X��Y�ֱ���12��32�������ӵĺ����������18�������ӵĽṹʾ��ͼ��
�����x��12������Y�����ԭ��������32����X��Y�ֱ���12��32�������ӵĺ����������18�������ӵĽṹʾ��ͼ�� ��
��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��һ�������� | B��һ���Լ��� | C�����������Ի���ԣ�Ҳ���������� | D������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����״���£�4.48 L N2��O2�Ļ������������ԭ����Ϊ0.4NA |
| B�������£�1.0 L 1.0 mol��L-1NaAlO2��Һ�к��е���ԭ����Ϊ2NA |
| C���ڱ�״���£�22.4 L������22.4 L���������е�ԭ������Ϊ2NA |
| D��0.1 mol Fe�μ�������ԭ��Ӧ��ת�Ƶĵ�����Ŀһ����0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������谷�ɶ��ַ�����ɣ����������ڻ��� |
| B�������谷����̼���⡢������Ԫ�ص�������Ϊ12��1��14 |
| C��ÿĦ�������谷�����к���ԭ�Ӹ���Ϊ15NA |
| D�������谷��Ħ������Ϊ126 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1:1:1 | B��1:2:3 | C��3:4:3 | D��3:2:1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1mol�κ�������������������ȣ����Ҳ��ԼΪ22.4L |
| B���ڱ�״���£�18 gH2O��ռ�����Լ��22.4L |
| C����g��mol-1Ϊ��λʱ������ֵ��Ħ����������Է������������ԭ��������� |
| D��ͬ������O2��O3��������ԭ������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1 mol����������������������ΪNA |
| B����ϩ��C2H4���ͻ����飨C3H6����ɵ�28 g��������к���2NA����ԭ�� |
C��1mol Na2O2�������NA��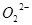 |
| D������0.1 mol�Ȼ����ı�����Һ�μӵ���ˮ�п���ȡ0.1NA�� Fe(OH)3������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com