
| A. | 1s22s22p63s13p3 | B. | 1s22s22p63s23p63d104s14p1 | ||
| C. | 1s22s22p63s23p63d24s2 | D. | 1s22s22p63s23p63d104s14p2 |
分析 A.先排满3s轨道,再排3p轨道;
B.先排满4s轨道,再排4p轨道;
C.电子填充顺序依次为1s2s2p3s3p3d4s;
D.先排满4s轨道,再排4p轨道.
解答 解:A.Si原子核外电子数为14,先排满3s轨道,再排3p轨道,核外电子排布式为:1s22s22p63s23p2,故A错误;
B.Zn原子核外30个电子,先排满4s轨道,再排4p轨道,核外电子排布式为:1s22s22p63s23p63d104s2,故B错误;
C.Ti原子核外22个电子,电子填充顺序依次为1s2s2p3s3p3d4s,则核外电子排布式为:1s22s22p63s23p63d24s2,故C正确;
D.Ga原子核外31个电子,先排满4s轨道,再排4p轨道,则核外电子排布式为:1s22s22p63s23p63d104s24p1,故D错误.
故选C.
点评 本题考查了原子核外电子排布,根据基态原子排布规律来分析解答即可,题目难度不大,侧重于考查学生对基础知识的应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
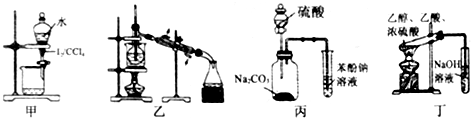
| A. | 装置甲:用CCl4萃取碘水中的碘 | |
| B. | 装置乙:加热碘的CCl4溶液,分离碘并回收CCl4 | |
| C. | 装置丙:验证硫酸、碳酸、苯酚溶液的酸性 | |
| D. | 用乙酸、乙醇制取乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀盐酸和Na2CO3 | B. | 稀盐酸和Na[Al(OH)4] | C. | CaCl2和Na2CO3 | D. | NaOH和AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 随着电子层数的增加单质的密度逐渐升高 | |
| B. | 随着核电荷数的增加单质的熔点逐渐降低 | |
| C. | 在自然界中都只能以化合态形式存在 | |
| D. | 单质都能与水反应,且反应后的溶液都呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
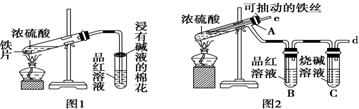
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com