
解析:同温同容时,气体的压强与气体的物质的量成正比。若只发生反应:
C+O2 ![]() CO2
CO2
0.25 mol 0.25 mol
容器内压强不变,即增大0倍。
若只发生反应:
![]() 2CO
2CO
0.25 mol 0.5 mol
容器内压强增大1倍。
因为0<0.4<1,所以以上两个反应同时发生。
方法一:平行计算法
设转化为CO的碳的物质的量为x,转化为CO2的碳的物质的量为y,则:
![]() 2CO
2CO
2 1 2
x 0.5x x
C+O2![]() CO2
CO2
1 1 1
y y y
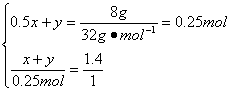
解得:![]()
所以m(C)=(x+y)×
方法二:碳原子守恒法
据题意可知,碳的物质的量=混合气(CO和CO2)的物质的量=1.4倍O2的物质的量
即:n(C)=1.4×![]() =0.35 mol
=0.35 mol
m(C)=0.35 mol×
答案:4.2 g


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的碳与8 g氧气置于一密闭容器中,使之在高温下反应,当恢复至原温度时,容器内压强比原来增大0.4倍,则参加反应的碳的质量为( )
A.2.4 g B.3 g C.4.2 g D.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com