
����Ŀ��һ���¶��£���1L�ܱ������м���1 mol HI(g)��������Ӧ2HI(g) ![]() H2(g)+I2(g)��H2���ʵ�����ʱ��ı仯��ͼ��ʾ��
H2(g)+I2(g)��H2���ʵ�����ʱ��ı仯��ͼ��ʾ��

��1��0~2 min�ڵ�ƽ����Ӧ����v(HI)=______________________�� ���¶��£�H2(g)+I2(g) ![]() 2HI(g)��ƽ�ⳣ��K=________��
2HI(g)��ƽ�ⳣ��K=________��
��2����ͬ�¶��£�����ʼ����HI(g)�����ʵ�����ԭ����2������_________ԭ����2����
a��ƽ�ⳣ�� b��HI��ƽ��Ũ��
c���ﵽƽ���ʱ�� d��ƽ��ʱH2���������
��3��ʵ������Zn��ϡ������ȡH2����Ӧʱ��Һ��ˮ�ĵ���ƽ��________�ƶ�������������ҡ������������������������Լ��е�_______������H2�����ʽ�����
a��NaNO3 b��CuSO4 c��Na2SO4 d��NaHSO3
��4��ij������ȼ�ϵ����CsHSO4����Ϊ����ʴ���H+��������ṹ��ͼ������ܷ�Ӧ�ɱ�ʾΪ2H2+O2===2H2O�������й�˵����ȷ����___________

A������ͨ�����·��b������a��
B��b���ϵĵ缫��ӦʽΪ��O2+2H2O+4e��=4OH��
C��ÿת��0.1mol���ӣ�����1.12L��H2
D��H+��a��ͨ�����������ʴ��ݵ�b��
���𰸡�0.1 mol��L��1��min��1 64 b ���� b D
��������
2HI(g) ![]() H2(g)+I2(g)
H2(g)+I2(g)
��ʼ��mol��1 0 0
ת����mol��0.2 0.1 0.1
ƽ�⣨mol��0.8 0.1 0.1
0��2min�ڵ�ƽ����Ӧ����v(HI)=![]() =0.1 mol��L��1��min��1��
=0.1 mol��L��1��min��1��
ƽ�ⳣ��K/=![]() = 1/64��
= 1/64��
��ӦH2(g)+I2(g) ![]() 2HI(g)��ƽ�ⳣ��K=1/K/=64��
2HI(g)��ƽ�ⳣ��K=1/K/=64��
��ˣ�������ȷ���ǣ�64��
��2������ʼ����HI��g�������ʵ�����ԭ����2�����൱���Ƚ�HI���뵽2L���������ٽ����ѹ����1L����Ϊ�÷�ӦΪ�������Ӧ����ѹƽ�ⲻ�ƶ�������HI��Ũ��Ϊԭ����2����H2������������䣻�¶Ȳ��䣬ƽ�ⳣ�����䣻����HI�����ʵ�������Ӧ��Ũ������Ӧ���ʼӿ죬�ﵽƽ���ʱ�����̡���ѡb��
��ˣ�������ȷ���ǣ�b��
��3��ˮ�������������Ӻ����������ӣ�������������ˮ���룬п�����ᷴӦ��������п��������������Ũ����С��ˮ�ĵ���̶�����������ˮ�ĵ���ƽ�������ƶ���
a������Һ�м���NaNO3��������Һ�к������ᣬ�����п��Ӧ��������������a����
b��CuSO4��п�����û���Ӧ����ͭ��ͭ��п��ϡ���ṹ��ԭ��أ������ܼӿ췴Ӧ���ʣ���b��ȷ��
c��Na2SO4��Ӱ�췴Ӧ���ʣ���c����
d��NaHSO3�����ᷴӦ���ɶ�������������Ũ�ȼ�С�������������������ʼ�С����d����
��ˣ�������ȷ���ǣ����ң�b��
��4��A. ����ͨ�����·�Ӹ�����������������a������b������A����
B. ����ʴ���H+����b���ϵĵ缫��ӦʽΪO2+4e��+4H+=2H2O ����B����
C.ÿת��0.1mol����������0.05mol��H2����״���µ�H21.12L����״̬δ֪�����ܼ����������C������
D. ԭ����У��������������ƶ�������H+��a��ͨ�����������ʴ��ݵ�b��������Dѡ������ȷ����
��ˣ�������ȷ���ǣ�D��


 һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������ͼ��ʾװ��(I)��ȡ�屽�������顣�ѣ�������Ϊ��ɫҺ�壬������ˮ���е�38��4�����۵�һ119�����ܶ�Ϊ1��64g��cm-3����Ҫʵ�鲽��������

����������Ժ�����ƿ�м���һ��������Һ����
������ƿ�м����Ҵ���ŨH2SO4�Ļ��Һ��ǡ��û���������ܿڡ�
�۽�Aװ���д���˿С�����²�����Һ�С�
�ܵ�ȼBװ���оƾ��ƣ���С������ƿ����10���ӡ�
����д���пհף�
��1��Aװ���з����ķ�Ӧ�Ļ�ѧ����ʽ________________________________
��2������a��������_______________��
��3��Cװ����U�ܵ��ڲ�������ˮ��ס�ܵ�������___________________________��
��4����Ӧ��Ϻ��������������ʱ��������Ҫ����������(ֻ��һ��)_____________��
��5��������пɷ��ô����ȣ�������____________________________________��
��6��Ϊ֤����ͱ���������Ӧ��ȡ�������Ǽӳɷ�Ӧ����ѧ����װ��(��)����װ��B��Cֱ����A���������·�Ӧ����ƿ��ʢ�ŵ�Һ��ΪAgNO3��Һ��
��װ��(��)����ƿ��С�Թ��ڵ�Һ����____________(������)��������Ϊ_______________
����֤����ͱ��ķ�Ӧ��ȡ����Ӧ������Ϊ_________________________��װ��(��)������������_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ���������ֵ������˵������ȷ����( )
��0.5molO3��11.2LO2�����ķ�����һ�����
�ڱ�״���£�22.4L��������������ַ�Ӧ��ת�Ƶĵ�����Ϊ3NA
��ͨ��״���£�NA ��CO2����ռ�е����Ϊ22.4L
�ܳ��³�ѹ�£�92g��NO2��N2O4������庬�е�ԭ����Ϊ6NA
�ݳ����£�4.4g CO2��N2O������Ӧ��������������е�ԭ����Ϊ0.3 NA
���ڷ�ӦKIO3��6HI===KI��3I2��3H2O�У�ÿ����3molI2ת�Ƶĵ�����Ϊ6NA
�߱�״����,22.4 L SO3���еķ�����ΪNA
���ڳ��³�ѹ�£�1 mol O2���е�ԭ����Ϊ2NA.
�����ʵ���Ũ��Ϊ0.5 mol��L-1 MgCl2��Һ��,����Cl������ΪNA
�⽫100 mL 0.1 mol��L-1��FeCl3��Һ�����ˮ�п��Ƶ�Fe(OH)3������ĿΪ0.01NA
A. �٢ڢܢ�B. �ܢݢ�C. �ۢޢ��D. �ܢݢ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʪ����п�ĵ��ѭ����Һ�У��ϸ�Ũ�ȵ�![]() �ḯʴ��������������ܺġ�������Һ��ͬʱ����Cu��CuSO4������CuCl�����Ӷ���ȥ
�ḯʴ��������������ܺġ�������Һ��ͬʱ����Cu��CuSO4������CuCl�����Ӷ���ȥ![]() ��������Һ��ƽ��ʱ�������Ũ�ȵĹ�ϵͼ������˵���������
��������Һ��ƽ��ʱ�������Ũ�ȵĹ�ϵͼ������˵���������

A. ![]() ��������Ϊ
��������Ϊ![]()
B. ��![]() ��ӦΪCu+Cu2++2
��ӦΪCu+Cu2++2![]() =2CuCl
=2CuCl
C. ����CuԽ�࣬Cu+Ũ��Խ�ߣ���![]() Ч��Խ��
Ч��Խ��
D. 2Cu+=Cu2++Cuƽ�ⳣ���ܴ�Ӧ������ȫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ֶ�����Ԫ��a��g���й���Ϣ���±���ʾ��
Ԫ�ر�� | a | b | c | d | e | f | g |
ԭ�Ӱ뾶/nm | 0.037 | 0.074 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
����ϼۻ���ͻ��ϼ� | +1 | ��2 | +3 | ��2 | +3 | +1 | +1 |
�����ƶϲ���ȷ���ǣ�������
A. �⻯���ȶ��Ե�ǿ����b��dB. �����Ե�ǿ����f��g
C. Ԫ��e��������ֻ�����ᷴӦD. Ԫ��a��Ԫ��d�γɵĻ��������ڹ��ۻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NOx����ҪָNO��NO2���Ǵ�����Ҫ��Ⱦ��֮һ����Чȥ�������е�NOx�ǻ�����������Ҫ���⡣
(1)��ˮ����NOx������Ȼ�ѧ����ʽ���£�
2NO2��g��+H2O��l��![]() HNO3��aq��+HNO2��aq�� ��H=116.1 kJ��mol1
HNO3��aq��+HNO2��aq�� ��H=116.1 kJ��mol1
3HNO2��aq��![]() HNO3��aq��+2NO��g��+H2O��l�� ��H=75.9 kJ��mol1
HNO3��aq��+2NO��g��+H2O��l�� ��H=75.9 kJ��mol1
��Ӧ3NO2��g��+H2O��l��![]() 2HNO3��aq��+NO��g������H=___________kJ��mol1��
2HNO3��aq��+NO��g������H=___________kJ��mol1��
(2)�����������£����ʹ���M�ܴ�NH3��NOx��Ӧ����N2���ֽ�һ��������O2��NH3��NOx�Ļ�����壬����ͨ��װ�д���M�ķ�Ӧ���з�Ӧ��

��Ӧ��ͬʱ��NOx��ȥ�����淴Ӧ�¶ȵı仯������ͼ��ʾ����50��250 �淶Χ�������¶ȵ����ߣ�NOx��ȥ������Ѹ��������������������Ҫԭ����______________________ ��
����Ӧ�¶ȸ���380 ��ʱ��NOx��ȥ����Ѹ���½���ԭ�������___________________ ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ����ѧ����ѧ�ۺ��������õĺϽ𣬹㷺Ӧ�������������Ԫ���������Ǵ�ij�Ͼ���ͭԪ��(��BeO25%��CuS71%������FeS��SiO2)�л������ͭ���ֽ��������̡�
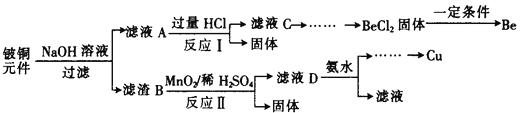
��֪��I���롢��Ԫ�ش������ڱ��еĶԽ���λ�ã���ѧ��������
���������£�Ksp[Cu(OH)2]=2.2��10![]() Ksp[Fe(OH)3]=4.0��10
Ksp[Fe(OH)3]=4.0��10![]() Ksp[Mn(OH)2]=2.1��10
Ksp[Mn(OH)2]=2.1��10![]()
(1)��ҺA����Ҫ�ɷֳ�NaOH�⣬����______________ (�ѧʽ)��
д����ӦI�к��뻯������������ᷴӦ�����ӷ���ʽ____________________________��
(2)��ҺC�к�NaCl��BeCl2������HCl��Ϊ�ᴿBeCl2��ѡ��������貢����___________��
a����������� NaOH b��ͨ�������CO2 c����������İ�ˮ
d������������HCl e������ f��ϴ��
(3)��MnO2�ܽ����������е���Ԫ������Ϊ������д����Ӧ����CuS������Ӧ�Ļ�ѧ����ʽ________________________________________________________��
������ŨHNO3�ܽ�������ȱ����______________ (��дһ��)��
(4)��ҺD�к�c(Cu2+)=2.2mol��L��1��c(Fe3+)=0.008mol��L��1��c(Mn2+)=0.01mol��L��1����μ���ϡ��ˮ����pH�����η��룬���ȳ�������________________ (�����ӷ���)��Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pHֵ����______________��ȡ��ͭԪ��1000g�����ջ��Be������Ϊ81g���������______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȸʯ��һ�ֹ��ϵ����ϣ�����������ͭ���ﹲ������ͭ��ͭ��ͭ����Ȼͭ�ȣ�����Ҫ�ɷ���Cu(OH)2CuCO3��������FeCO3����������ʵ�����Կ�ȸʯΪԭ���Ʊ�����ͭ����IJ������£�

��֪��Fe3+��ˮ��Һ�д���Fe3++3H2O![]() Fe(OH)3+3H+
Fe(OH)3+3H+
Fe(OH)3��ʼ������pH=2.7��������ȫ��pH=3.7��
(1)Ϊ�����ԭ�ϵĽ������ʣ��ɲ�ȡ�Ĵ�ʩ��________��
(2)����I���ó�����Ҫ�ɷֵ���;Ϊ________��
(3)��������Լ�����____________(����ţ�
A.KMnO4 B.H2O2 C.Fe�� D.KSCN
�����Լ��ٷ�Ӧ�����ӷ���ʽΪ��________��
(4)�����ʵ�������Һ3���Ƿ����Fe3+��___________��
(5)�ⶨ����ͭ����(CuSO4xH2O)�нᾧˮ��xֵ����ȡ2.4500g����ͭ���壬�������������ٸı�ʱ��������ĩ������Ϊ1.6000g��������x=______����������ȷ��0.1)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ����֤ľ̿�ɱ�Ũ����������CO2��ѡ����ͼ��ʾװ��(�ں�����)����ʵ�顣

��1���簴�����������ҵ�����������ͼ��ʾװ�õ���ȷ˳����_______(����ĸ��
��2����ʵ��������CO2���ɣ���װ���ҡ����е�����ֱ�Ϊװ������______��װ�ñ���________��
��3��װ�ö�������KMnO4��Һ��������________��
��4��д��װ�ü�����������Ӧ�Ļ�ѧ����ʽ��________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com