

分析 啧啧啧A生成氯气,氯气含有杂质气体,通过装置B中的饱和食盐水除去氯气中的氯化氢气体,装置C 可以使气体混合均匀,浓硫酸具有吸水性,能够干燥混合气体,装置D发生有机反应R-H+Cl2?R-Cl(液)+HCl(气),装置E中碘化钾能够与过量的氯气发生反应生成氯化钾和单质碘,用来吸收过量的氯气,装置中最后剩余的氯化氢气体需要吸收不能排放到空气中,氯化氢易溶于水需要防止倒吸,F装置在吸收氯化氢时可防止倒吸,
(1)浓盐酸易挥发,制备的氯气中含有挥发的氯化氢;氯化氢易溶于水,氯气在饱和食盐水中的溶解度较小;
(2)碘化钾能够与过量的氯气发生反应生成氯化钾和单质碘,用来吸收过量的氯气;
(3)甲烷和氯气发生取代反应,产物为氯化氢和一氯甲烷、二氯甲烷、三氯甲烷和四氯化碳;最后生成的HCl溶于水生成盐酸,与有机物可用分液的方法分离;
(4)避免空气干扰需要先通入甲烷气体排净装置内空气,然后加热装置A反应得到氯气,装置C中装有浓硫酸能够干燥混合气体,能够使氯气与甲烷混合均匀,加热装置D;
解答 解:(1)浓盐酸易挥发,制备的氯气中含有挥发的氯化氢;氯化氢易溶于水,氯气在饱和食盐水中的溶解度较小,可以用饱和食盐水除去氯气中的氯化氢,
故答案为:饱和食盐水;
(2)碘化钾能够与过量的氯气发生反应生成氯化钾和单质碘,用来吸收过量的氯气;
故答案为:除去未反应完的Cl2 ;
(3)甲烷和氯气发生取代反应,产物为氯化氢和一氯甲烷、二氯甲烷、三氯甲烷和四氯化碳;其中一氯甲烷为气态,二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,E装置中除了有盐酸生成外,还含有二氯甲烷、三氯甲烷和四氯化碳,二氯甲烷、三氯甲烷和四氯化碳不溶于水,能分层,可用分液分开,
故答案为:分液;
(4)为避免空气干扰需要先通入甲烷气体排净装置内空气,然后加热装置A反应得到氯气,装置C中装有浓硫酸能够干燥混合气体,能够使氯气与甲烷混合均匀,气泡冒出后再加热装置D,这三种操作的先后顺序是:③①②,
故答案为:③①②.
点评 本题考查了甲烷和氯气的取代反应、氯气的实验室制法,熟悉反应原理是解题关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
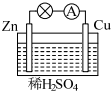 如图所示是 Zn和 Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )
如图所示是 Zn和 Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )| A. | ①②③ | B. | ②④⑥ | C. | ③④⑤ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL,1mol•L-1 的NaCl | B. | 100mL,2mol•L-1 的MgCl2 | ||
| C. | 100mL,1mol•L-1 的FeCl3 | D. | 50mL,3mol•L-1 的FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
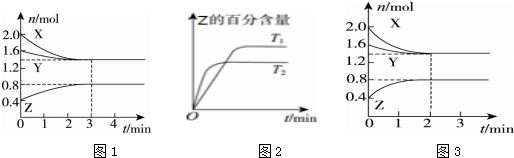
| A. | 容器中发生的反应可表示为3X(g)+Y(g)═2Z(g) | |
| B. | 反应进行的前3 min内,用X表示的反应速率v(X)=0.2 mol/(L•min) | |
| C. | 保持其他条件不变,升高温度,反应的化学平衡常数K减小 | |
| D. | 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(W)=v(Z) | B. | 2v(X)=3v(Z) | C. | v(X)=2v(Y) | D. | 3v(W)=2v(X) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
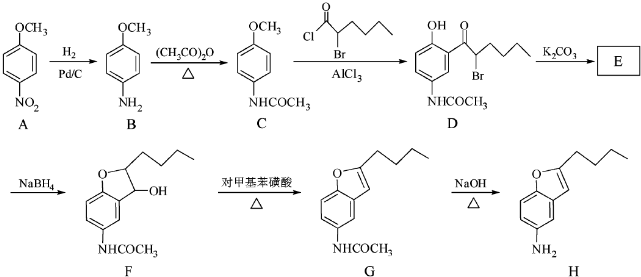
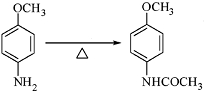 +CH3COOH
+CH3COOH .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L NO2溶于水完全反应转移电子数为0.2NA | |
| B. | 标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5NA | |
| C. | 氢原子数为0.6NA的乙烯分子中含有的π键数为0.2NA | |
| D. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO | B. | NO2 | C. | N2O | D. | N2O3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com