
分析 (1)根据n=$\frac{m}{M}$计算碳酸钠物质的量,再根据c=$\frac{n}{V}$计算c(Na2CO3);
(2)溶液中c(Na+)=2c(Na2CO3)来计算溶液Na+的物质的量浓度;
解答 解::(1)碳酸钠物质的量=$\frac{10.6g}{106g/mol}$=0.1mol,故溶液中c(Na2CO3)=$\frac{0.1mol}{1L}$=0.1mol/L,答:该溶液中Na2CO3的物质的量浓度为0.1mol/L;
(2)溶液中c(Na+)=2c(Na2CO3)=0.1mol/L×2=0.2mol/L,答:液Na+的物质的量浓度为0.2mol/L.
点评 本题考查物质的量浓度有关计算,比较基础,注意对公式的理解与灵活应用.


科目:高中化学 来源: 题型:实验题
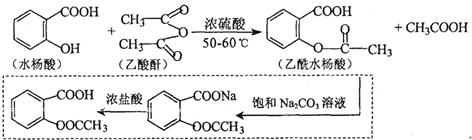
 .
. .
.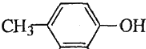 也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe+CuSO4=FeSO4+Cu | B. | Cl2+H2O=HCl+HClO | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | AgNO3+HCl=AgCl↓+HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 共价键 | H-H | N≡N | H-N |
| 键能(kJ•mol-1) | 436 | 945 | 391 |
| 装置 | 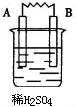 | 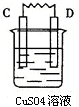 | 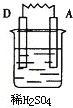 | 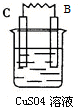 |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 | 金属B不断溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 名称 | 分子式 | 结构式 | 结构简式 |
| 乙烯 | C2H4 |  | \ |
| 丙烯 | C3H6 | \ | CH3-CH=CH2 |
| 乙炔 | \ | H-C≡C-H | |
| 异丁烷 | \ | CH3CH(CH3)CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .化合物
.化合物 是合成药物的中间体,请写出以有机物A和
是合成药物的中间体,请写出以有机物A和 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com