
室温下向10 mL pH = 3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中C(CH3COO-)/C(CH3COOH).c(OH-)不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH = 11的NaOH溶液,混合液pH=7
B
【解析】
试题分析:醋酸属于弱酸,加水稀释有利于醋酸的电离,所以醋酸的电离程度增大,同时溶液中导电粒子的数目会增大,由于溶液体积变化更大,所以溶液的酸性会降低,即c(H+)、c(CH3COO-)、c(CH3COOH)均会降低,因此选项A、C均不正确;由水的离子积常数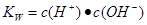 知
知 ,所以
,所以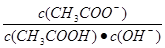 =
=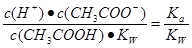 其中
其中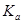 表示醋酸的电离平衡常数,由于水的离子积常数和醋酸的电离平衡常数均只与温度有关,所以选项B正确;pH=3的醋酸说明醋酸的浓度大于0.001mol/L,pH=11的NaOH溶液说明氢氧化钠的浓度等于0.001mol/L,因此加入等体积的pH=11的NaOH溶液时,醋酸会过量,溶液显酸性,D不正确,答案选B。
表示醋酸的电离平衡常数,由于水的离子积常数和醋酸的电离平衡常数均只与温度有关,所以选项B正确;pH=3的醋酸说明醋酸的浓度大于0.001mol/L,pH=11的NaOH溶液说明氢氧化钠的浓度等于0.001mol/L,因此加入等体积的pH=11的NaOH溶液时,醋酸会过量,溶液显酸性,D不正确,答案选B。
考点:考查外界条件对醋酸电离平衡的影响
点评:该题是高考中的常见题型,属于中等难度的试题。主要是考查学生对弱电解质电离平衡以及影响电离平衡因素的熟悉了解程度,有利于培养学生的逻辑推理能力和创新思维能力。明确温度与电离平衡常数的关系、溶液的pH与物质的量浓度的关系、稀释中溶液体积的变化与离子的物质的量的变化程度是解答本题的关键。


科目:高中化学 来源:2015届江苏无锡一中高二上学期期中考试化学试卷(选修)(解析版) 题型:选择题
室温下向10 mL c(H+)=10-3 mol·L-1的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中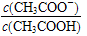 变大
变大
C.醋酸的电离程度增大,c(OH-)亦增大
D.再加入10 mL c(OH-)=10-3 mol·L-1的NaOH溶液,醋酸与NaOH恰好完全反应
查看答案和解析>>
科目:高中化学 来源:2013-2014学年上海市长宁区高三上学期期末(一模)考试化学试卷(解析版) 题型:选择题
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH <7
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省瑞安十校高三上学期期末联考理综化学试卷(解析版) 题型:选择题
下列有关叙述正确的是 ( )
A.氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+)
B.pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+)
C.室温下向10 mL pH=3的醋酸溶液中加水稀释,溶液中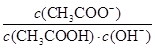 不变
不变
D.在0.1 mol·L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源:2011-2012学年陕西省兴平市高三上学期期末练习化学试卷 题型:选择题
室温下向10 mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中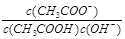 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com