
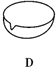
【题目】回答下列问题:如图所示是分离混合物时常用的仪器,回答下列问题:
![]()
![]()
![]()
![]()
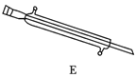
(1)写出仪器A、E的名称__、__。
(2)若向C装置中加入碘水和少量CCl4,振荡后静置,会观察到的现象是__。
(3)若粗盐溶液中含有少量的CaCl2、MgCl2、MgSO4,为除掉这些杂质,需依次加入的化学试剂是NaOH、__、__、HCl(写化学式)。
【答案】蒸馏烧瓶 冷凝管 分层,下层液体呈紫红色 BaCl2 Na2CO3
【解析】
(1)根据仪器的构造可知,仪器A、E的名称分别为蒸馏烧瓶、冷凝管;
(2)若向C装置(分液漏斗)中加入碘水和少量CCl4,振荡后静置,由于单质碘易溶于四氯化碳中,且四氯化碳密度大于水,会观察到的现象是分层,下层液体呈紫红色;
(3)若粗盐溶液中含有少量的CaCl2、MgCl2、MgSO4,为除掉这些杂质,利用氢氧化钠除去镁离子、利用钙离子除去碳酸根离子、利用钡离子除去硫酸根离子,试剂应过量,且碳酸钠应在钡离子后加入以保证过量的钡离子用碳酸钠除去,故需依次加入的化学试剂是NaOH、BaCl2、Na2CO3、HCl。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某小组对某无色水样进行检验,已知水样中只可能含有K+、Mg2+、Cu2+、Al3+、CO32-、SO42-、C1-中的若干种离子。该小组取100mL水样进行实验,先滴加硝酸钡溶液,再滴加1mol·L-1的硝酸,实验过程中沉淀质量变化情况如图所示,下列分析错误的是

A. 一定含有的离子是:K+、SO42-、CO32-
B. BC段反应的离子方程式:BaCO3+2H+=Ba2++CO2↑+H2O
C. K+物质的量浓度的范围是: c(K+)≥0.6mol/L
D. 取少量水样置于试管中,滴加硝酸银溶液,可检验水样中是否含有C1-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断开1 mol Cl2(g)中Cl-Cl键需要吸收243 kJ能量。根据能量变化示意图,下列说法或热化学方程式正确的是

A.H2(g)+Cl2(g)=2HCl(g) △H=-185 kJ·mol-1
B.生成1 mol H2(g)中的H-H键放出121.5 kJ能量
C.断开1 mol HCl(g)中的H-Cl键要吸收864 kJ能量
D.HCl(g)=![]() H2(g)+
H2(g)+![]() Cl2(g) △H=-92.5 kJ·mol-1
Cl2(g) △H=-92.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如下图所示:
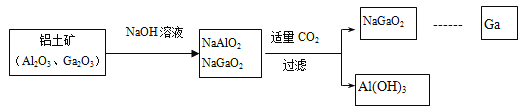
下列判断不合理的是:
A. Al、Ga均处于IIIA族
B. Ga2O3可与盐酸反应生成GaCl3
C. Ga(OH)3可与NaOH反应生成NaGaO2
D. 碱性:Al(OH)3>Ga(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某反应的微观示意图,下列有关说法不正确的是

A. 生成的物质都是氧化物
B. 反应前后原子的种类不变
C. 该反应的基本类型属于置换反应
D. 反应方程式为2H2S+3O2 ![]() 2SO2+2H2O
2SO2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式_______
(2)某炔烃和氢气充分加成生成2,5﹣二甲基己烷,该炔烃的结构简式是_______
(3)某芳香烃结构为![]() 。它一氯代物有_______种。
。它一氯代物有_______种。
(4)分子式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为_______,若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为_______。
(5) 分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,该芳香烃的结构简式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,科学家通过对稻壳进行控制性焚烧热解,从中提取一种叫做生物质纳米结构二氧化硅的超高活性材料,将少量这种材料掺入混凝土中,即可轻易制备出超高强度和超高耐久性能的高性能混凝土。关于二氧化硅下列说法中正确的是( )
A.二氧化硅溶于水显酸性,所以二氧化硅属于酸性氧化物
B.二氧化碳通入硅酸钠溶液中可以得到硅酸
C.由CaCO3+SiO2![]() CaSiO3+CO2↑可知硅酸的酸性比碳酸强
CaSiO3+CO2↑可知硅酸的酸性比碳酸强
D.二氧化硅是酸性氧化物,它不溶于任何酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M(C16H14O2)是一种香料,工业上利用烃A和甲苯为主要原料,按下列路线合成:

已知:①气态烃A在标准状况下的密度是1.25g/L,能作为果实催熟剂;②醛在碱性溶液中能发生羟醛缩合反应,再脱水生成不饱和醛:RCH2CHO+ 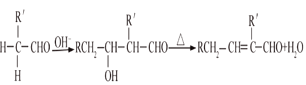 。请回答下列问题:
。请回答下列问题:
(1)K的名称是___________;G中含有的官能团名称是______________。
(2)写出D→E的化学方程式____________________________________。
(3)A→B的反应类型是_______;
(4)同时满足下列三个条件的K的同分异构体有_____种(不考虑立体异构)。①遇FeCl3溶液发生显色反应;②能发生银镜反应;③除苯环以外不再含有其他环状结构。其中核磁共振氢谱为五组峰的结构简式为____。
(5)以乙醇为起始原料,选用必要的无机试剂设计合成1-丁烯的路线。(用结构简式表示有机物,箭头上注明试剂和反应条件)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族,e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是_____(填元素符号),e的价层电子轨道表示式为____。
(2)a和其他元素形成的二元共价化合物中,三角锥形分子的中心原子的杂化方式为____。
(3)这些元素形成的含氧酸中,HNO2、H2SO3的中心原子价层电子对数之和为____,H2SO3和H2SO4酸根的空间构型分别为____、____。
(4)e单质晶体结构如图1,此晶胞模型名称为____,e原子半径为r cm,e的相对原子质量为M,晶胞密度为ρ g/cm3,则阿伏加德罗常数为_____mol-1(用r、ρ表示)。
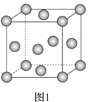
(5)这5种元素形成的一种1∶1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。
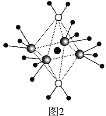
该化合物中,阴离子为____,阳离子中存在的化学键类型有______;该化合物加热时首先失去的组分是______(填“H2O”或“NH3”),判断理由是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com