
| A. | 四种元素的原子中,原子半径最大的是Z | |
| B. | X、Y形成的化合物能溶于盐酸 | |
| C. | 1 mol W单质与足量X单质反应,转移的电子数为2NA | |
| D. | Z 的最高价氧化物对应水化物的酸性强于Y的最高价氧化物对应水化物的酸性 |
分析 Y原子的最外层电子数与核外电子总数之比为2:7,若最外层电子数为2,则核外电子总数为7,为N原子,最外层电子数为5,不满足题意;若最外层电子数为4,则核外电子总数为14,为硅元素,满足条件;若最外层电子数为6,最外层电子总数为42,该元素不是短周期元素;所以Y为Si;W和Z的原子序数之和为:14×2=28;W、X、Z三种元素形成的某种化合物能消毒杀菌,说明该化合物具有强氧化性,常见的具有强氧化性的物质中含有Cl、O;氯元素与氧元素的原子序数之和为25,不满足题意,如果W和Z中有一种为O,则另一种元素的原子序数为20,为Ca元素,不属于短周期;如果W和Z中有一种为Cl,则另一种为钠,W和Z形成的化合物为氯化钠,满足题意,所以Y为Si、X为O、W为Na、Z为Cl,据此进行解答.
解答 解:根据分析得出:X为O、Y为Si、Z为Cl、W为Na,
A.电子层多一般半径大,同周期序数越小半径越大,则四种原子中,Na的原子半径最大,即原子半径最大的是W,故A错误;
B.X为O、Y为硅,二者形成的化合物为二氧化硅,二氧化硅不溶于盐酸,故B错误;
C.W为钠,X为O,1mol钠与足量氧气完全反应失去了1mol电子,转移的电子数为NA,故C错误;
D.Z为Cl、Y为Si,二者非金属性大小为:Cl>Si,所以最高价氧化物对应的水化物酸性大小为:Z>Y,故D正确;
故选:D.
点评 本题为无机推断,侧重考查了原子结构相关知识,题目难度中等,明确原子结构及常见单质及其化合物性质是解答本题关键,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:选择题
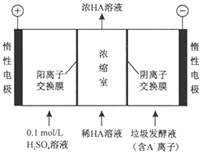 对生活污水进行处理是防止水体污染、改善水质的主要措施.电渗析法处理厨房垃圾发酵液(含污染物乳酸跟离子)同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子).下列叙述中正确的是( )
对生活污水进行处理是防止水体污染、改善水质的主要措施.电渗析法处理厨房垃圾发酵液(含污染物乳酸跟离子)同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子).下列叙述中正确的是( )| A. | 阴极区溶液的pH变小 | |
| B. | 阳极的电极反应式为2H2O-4e-═4H++O2↑ | |
| C. | 通过一段时间后浓缩至水的量减少,导致乳酸溶液浓度上升 | |
| D. | 若阳、阴离子交换膜调换位置,与如图可以达到相同的效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | T℃时,pH=6的纯水中,含1×10-6NA个OH- | |
| B. | 标准状况下,1 L pH=13的氢氧化钡溶液中n(OH-)为0.1NA | |
| C. | 室温下,14.0 g乙烯和丁烯的混合气体中含有的C-H键数目为2.0NA | |
| D. | 0.1 mol Cu与足量热的浓硫酸反应生成SO2的体积约为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的液化是物理变化 | |
| B. | 纤维素水解产物可以通过一系列化学变化制乙醇 | |
| C. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| D. | 漂白粉长期放置会被空气中的氧气氧化而变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
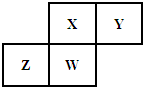 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是内层电子数的三倍.下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是内层电子数的三倍.下列说法不正确的是( )| A. | Y元素与氢元素可形成H2Y2型的离子化合物 | |
| B. | Z元素的单质有半导体特性,原子半径:Z>X | |
| C. | 最高价氧化物对应水化物的酸性:HXO3>H3WO4 | |
| D. | 元素Z、W的最高正价分别与其主族序数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | 元素的相关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 原子的M电子层上有3个电子 |
| C | 在短周期主族元素中,其原子半径最大 |
| D | 其最外层电子数是电子层数的2倍,且低价氧化物能与其气态氢化物反 应生成D的单质和H2O |
| E | 元素最高正价与最低负价的代数和为6 |
| A. | A的气态氢化物具有还原性,常温下,该氢化物水溶液的pH>7 | |
| B. | C单质在氧气中燃烧后的产物中阴阳离子个数之比为1:2 | |
| C. | 在B和E所形成的化合物中存在离子键 | |
| D. | C与D可形成不同原子或离子个数比的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟基的电子式: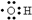 | B. | 淀粉和纤维素的实验式:CH2O | ||
| C. | CH4分子的球棍模型: | D. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
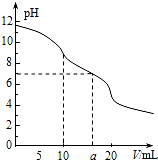 常温下,用 0.1mol•L-1 HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用 0.1mol•L-1 HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )| A. | 当V=0时:c(CO32-)>c(HCO3-)>c(OH-)>c(H2CO3) | |
| B. | 当V=5时:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+) | |
| C. | 当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能够节约原料和能源 | B. | 能提高产品的产量 | ||
| C. | 能够提高化学反应速率 | D. | 能够提高经济效益 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com