
【题目】短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如下图所示。R原子最外层 电子数是电子层数的2倍,Y 与Z 能形成Z2Y、Z2Y2 型离子化合物, Z 与T形成的化合物Z2T。下列推断错误的是
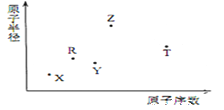
A. 形成的简单离子半径的大小顺序为T>Y>Z
B. Z2Y、Z2Y2所含有的化学键类型相同
C. 0.005mol·L-1T的最高价氧化物对应水化物的水溶液pH等于2
D. Z2T的水溶液显碱性,对水的电离有促进作用
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是 ( )
A. 二氧化硅与强碱溶液反应: SiO2+2OH- = SiO32-+ H2O
B. 将氯气通入NaOH溶液中:Cl2 + OH-= Cl-+ HClO
C. 金属钠与水反应:Na+2H2O=Na+ + 2OH-+ H2↑
D. 少量的金属锌加入到FeCl3溶液中: 2Fe3++3Zn = 2Fe+3Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石等混合物。某化学兴趣小组从铁砂中分离出磁性氧化铁,并进行铝热反应实验。
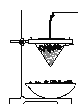
(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是______________,
现象很壮观,取少许反应生成的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现这种结果的原因,除了可能混有没反应的磁性氧化铁外,还有一个原因是 。
(2)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝。该实验所用试剂是_________,反应的离子方程式为___________________________________________。
(3)请写出此铝热反应的化学方程式: 。
每摩铝参与反应,转移的电子数为 。
(4)生成除磁性氧化铁可做铝热反应实验外,下列哪些试剂也可以________。
A.CuO B.Na2O2 C.MnO2 D.MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.氯气、液氯和氯水是同一种物质,只是状态不同,都属于纯净物
B.氯气是纯净物,氯水是混合物
C.铁丝在氯气中燃烧生成黄色固体FeCl2
D.新制的氯水只含有氯气分子和水分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种含硅元素的物质之间的相互转化关系如图所示:

(1)写出图示反应的几种物质的化学式:B________,C________,D________。
(2)写出下列反应的化学方程式:①B→A:______________________________;
②B→E:_____________________________________________________。
(3)写出下列溶液中反应的离子方程式:D→C___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气中常含有H2S 等有毒气体,下面是以天然气为原料合成氨的工艺流程图。(反应条件已略去)
请根据图回答下列问题。
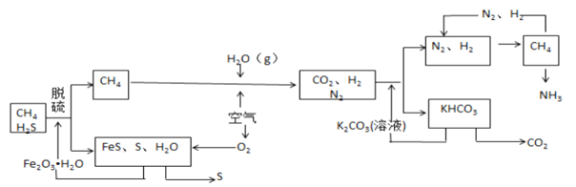
(1)将天然气直接燃烧,产生的有害物质是______________,,引起的环境问题是___________________。
(2)从空气中分离出O2 的方法是______________。
(3)一定条件下发生脱硫反应的化学方程式是_______________________。
(4)上图流程中K2CO3溶液的作用是________________,该反应的离子方程式是_____________。
(5)工业合成氨的化学方程式是_____________,生成的氨气可用于____________(写一条)。
(6)该工艺流程中有多处循环,参与循环的物质有N2、H2、___________和_____________等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用自来水养鱼时,通常先将自来水晒一段时间后再注入鱼缸,目的是 ( )
A.提高水温 B.增加水中氯气的含量
C .除去水中少量的次氯酸 D.用紫外线杀死水中的细菌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、A12O3,不考虑其他杂质)制取FeSO4·7H2O,其制备工艺流程如下:
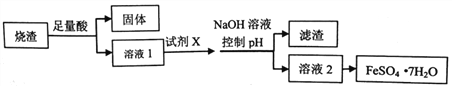
结合所学知识回答:
(1)溶解烧渣选用的酸应为_____(填化学式),选用的试剂X为_____(填试剂名称)。
(2)加入NaOH控制pH的目的是____________。
(3)从溶液2得到FeSO4·7H2O的实验操作主要步骤是________________________。
(4)为了测定获得的绿矾产品的纯度,进行了如下实验操作:
I.称取2.850g绿矾产品,溶解,用250mL容量瓶配制成待测液;
II.量取25.00mL待测溶液置于锥形瓶中;
III.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为 20.00mL。
①判断此滴定实验达到终点的方法是____________。
②该滴定反应的离子方程式为___________________。
③上述样品中FeSO4·7H2O的纯度为____________________。
(5)古代炼丹家以绿矾(FeSO4·7H2O)为原料,放在炼丹炉中锻烧可制得绿矾油。下图是2.780 g绿矾隔绝空气受热分解时,所得固体产物的质量随温度变化的曲线。将加热产生的所有气体通入足量的BaCl2溶液,得到白色沉淀1.165 g。则t1~t2段发生反应的化学方程式为__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且![]() 的值与温度高低有关。当n(KOH)=a mol,下列有关说法错误的是( )
的值与温度高低有关。当n(KOH)=a mol,下列有关说法错误的是( )
A.若某温度下,反应后![]() =11,则溶液中
=11,则溶液中![]() =
=![]()
B.参加反应的氯气的物质的量等于![]() a mol
a mol
C.改变温度,反应中转移电子的物质的量ne的范围:![]() a mol≤ne≤
a mol≤ne≤![]() a mol
a mol
D.改变温度,产物中KClO3的最大理论产量为![]() a mol
a mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com