
(10分)下图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

⑴该浓盐酸中HCl的物质的量浓度为 mol·L-1 。
⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取 体积的多少而变化的是。
体积的多少而变化的是。
A、溶液中HCl的物质的量 B、溶液的浓度
C、溶液中Cl-的数目 D、溶液的密度
⑶某学生欲用上述浓盐酸和蒸馏水配制500 ml 物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取 ml 上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
I、用量筒量取浓盐酸时仰视观察凹液面( )
II、定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水( )
③该36.5%的浓盐酸,若加入等质量的水稀释后,质量分数 18.25%;若加入等体积的水稀释后,质量分数 18.25%(用“小于”或“等于”或“大于”来填空)
(1)11.9 (2)BD (3) ①16.8; ② A; B ③等于 大于
【解析】(1)根据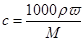 可知,盐酸的浓度是
可知,盐酸的浓度是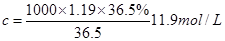 。
。
(2)由于溶液是均一、稳定的,所以取任意体积盐酸,其浓度和密度是不变的,但溶质的物质的量是变化的,答案选BD。
(3)①500 ml 物质的量浓度为0.400 mol·L-1的稀盐酸中溶质是0.5L×0.400mol/L=0.200mol。所以需要浓盐酸的体积是0.200mol÷11.9mol/L=0.0168L=16.8ml。
②根据c=n/V可知,若用量筒量取浓盐酸时仰视观察凹液面,则浓盐酸的体积偏大,结果偏大,答案选A;定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水,则容量瓶中溶液的体积偏大,浓度偏小,答案选B。
③溶液的质量变为原来的2倍,则质量分数是原来的1/2,即质量分数等于18.25%;由于盐酸的密度大于水的,所以加入等体积的水时,溶液的质量小于原来的2倍,则质量分数大于原来的1/2。


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g/mL HCl的质量分数:36.5%(1)该浓盐酸中HCl的物质的量浓度为 11.9mol/L 11.9mol/L .(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 BD BD (填编号).A.溶液中HCl的物质的量B.溶液的浓度C.溶液中Cl-的数目D.溶液的密度 (3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol/L的稀盐酸.该该学生需要量取 16.8 16.8 mL(小数点后保留一位)上述浓盐酸进行配制.②现有a.10mL量筒;b.25mL量筒;c.烧杯;d.托盘天平.e.500mL容量瓶;f.胶头滴管;g.玻璃棒,请从其中选取必要的仪器,按各仪器第一次使用先后顺序排序: bcgef或bfcge bcgef或bfcge (填编号).③在配制过程中,下列实验操作对所配制盐酸物质的量浓度有何影响?(在空格中填“偏高”、“偏低”或“无影响”):定容时俯视观察 偏高 偏高 ;定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水偏低 偏低 .
查看答案和解析>> 科目:高中化学 来源: 题型: (A类)试回答下列问题: (1)已知24克A和40克B恰好完全反应生成0.4molC和32克D,则C的摩尔质量为 80g/mol 80g/mol ;(2)将1molNa和lmol Mg分别投入到过量的盐酸中,分别得到溶液a和b,则溶液a和b的质量大小关系为ma = = mb;(3)下图为实验室某浓盐酸试剂瓶的标签上的有关数据,试根据标签上的有关数据回答下列问题:
|